Какие бывают операции на легких? Хирургическое лечение туберкулеза легких Как делают операцию расширению бронхов
Легкие – уникальный парный орган, обеспечивающий весь наш организм жизненно необходимым кислородом и выводящий из него углекислоту. И хотя они часто подвержены различным заболеваниям, их компенсаторные возможности велики, а ткань очень пластична. Это позволяет выполнять различные оперативные вмешательства, вплоть до полного удаления одного легкого.
Легкие имеют уникальное строение. За счет наличия полумиллиарда альвеол (дыхательных пузырьков) орган весом всего в 1 килограмм имеет общую дыхательную поверхность площадью в 100-150 квадратных метров, что можно сравнить с площадью теннисного корта. За сутки эта поверхность пропускает и «кондиционирует» более 10 000 литров воздуха. Длина же дыхательных путей, то есть разветвленного бронхиального дерева составляет около 3 000 километров. Более того, количество крови, проходящей через легкие в сутки, составляет 6-7 тонн!
Легкие, как и сердце, работают «на автомате», этот процесс регулируется сложным нейро-гуморальным механизмом. И хотя сердечную деятельность мы не можем на время остановить усилием воли, как дыхание, но и его остановка кратковременна, потому что включаются автоматические механизмы вдоха, уже независимо от нашей воли.
В альвеолах легких существует так называемый запас воздуха объемом около 200 мл. В экстренных ситуациях он включается в процесс дыхания, а в норме периодически обновляется в виде глубоких вздохов и зеваний.
Болезни легких, при которых нужна операция
К сожалению, далеко не все болезни легких можно вылечить с помощью медикаментов и процедур. Многие из них лечатся только хирургическим путем:

Все эти операции выполняются в специализированных отделениях торакальной (грудной) хирургии специалистами высокой квалификации.
Совет: часто самые опасные болезни легких, в том числе и рак, могут начинаться с безобидного, казалось бы, кашля. Его нельзя игнорировать, необходимо обратиться к врачу и пройти обследование.
Виды операций на легких
Все вмешательства на легких можно разделить на 2 группы по объему: пульмонэктомия или пневмонэктомия (полное удаление легкого) и резекция (удаление части легкого). Полное удаление выполняется в случаях злокачественных опухолей, а также при множественных патологических очагах во всех долях органа.
Резекция легких может быть различного объема:
- атипичная или краевая – удаление ограниченного участка на периферии;
- сегментэктомия – удаление сегмента с соответствующим сегментарным бронхом;
- лобэктомия – удаление одной доли;
- билобэктомия – удаление 2-х долей;
- редукция – уменьшение объема легких при поражении их эмфиземой (нефункционирующие воздушные полости в ткани органа).

По технологии все вмешательства бывают 2-х видов: торакотомические или традиционные - с широким вскрытием грудной клетки, и торакоскопические – малоинвазивные, выполняемые с помощью эндовидеотехники.
К хирургическим процедурам также относится торакоцентез – . Он может выполняться иглой, как и , или же путем небольшого надреза с введением дренажной трубки для оттока жидкости (гноя, крови), для введения лекарств.
Наконец, самая сложная операция – пересадка легких, которая сегодня довольно часто выполняется как за рубежом, так и в крупных отечественных клиниках в случаях, когда из строя выходят оба легких.
Современные технологии легочной хирургии
Благодаря появлению уникальных инновационных хирургических технологий, многие операции на легких выполняются сегодня малоинвазивным методом через несколько небольших надрезов на коже длиной не более 3 см. Технология подобна через небольшие надрезы с видеокамерой. В принципе, технология торакоскопических операций такая же, как и при лапароскопических вмешательств на органах брюшной полости ( , кишечника, и другие).
Такие операции гораздо менее травматичны, непродолжительны по времени, не требуют длительной госпитализации, и период реабилитации значительно короче.
Среди инновационных методов применяется также лазерная хирургия – для удаления опухолей, в том числе и рака, а также радиохирургия, криодеструкция (замораживание). Все эти технологии выполняются малоинвазивно - посредством чрескожной пункции, бронхоскопии или торакоскопии.
Совет: если предстоит операция на легких, необходимо заранее отказаться от курения и выполнять дыхательную гимнастику, чтобы легкие смогли очиститься. У курильщиков гораздо чаще возникают послеоперационные осложнения.
Послеоперационная реабилитация

Удаление легкого или его части неизбежно приводит к нарушению дыхательной функции и кислородного обмена всего организма. Основной задачей восстановительного периода является - «раздышать» оставшийся объем легких, с учетом их компенсаторных возможностей и обеспечить нормальный газообмен.
В раннем послеоперационном периоде в стационаре применяются специальные методы – аппаратные, медикаментозные, ЛФК, ингаляции – по индивидуальным схемам для каждого больного. После выписки эти задачи возлагаются на самого пациента. Основными мероприятиями являются:
- общегигиеническая гимнастика;
- специальная дыхательная гимнастика;
- посещение физиотерапевтических процедур, ингаляции;
- соблюдение диеты с достаточным содержанием белка и витаминов;
- регулярные прогулки на свежем воздухе.
Операции на легких сегодня выполняются по новым щадящим технологиям, а в сочетании с профессиональной послеоперационной реабилитацией они дают хорошие результаты восстановления функции дыхания.
Видео
Внимание! Информация на сайте представлена специалистами, но носит ознакомительный характер и не может быть использована для самостоятельного лечения. Обязательно проконсультируйтесь врачом!
отрезком резецированной на протяжении 7 см левой легочной артерии и передней стенкой ствола легочной артерии (рис. 74). Легкое распра вилось, артерия хорошо пульсирует. Антибиотики и два дренажа в, плевральную полость. Швы на рану грудной стенки.
Бронхоскопия: в области соустья хорошая адаптация краев слизи стой оболочки, просвет анастомоза не сужен.
Макропрепарат: доля плотная, с обрывками спаек. В корне ее плотные лимфатические узлы размером до 5X3 см. Ткань легкого на
Рис. 75. Тот же больной. Ангиопульмонограмма через l"/a месяца после операции. Сосуды оставшейся доли левого легкого хорошо контрастируются.
разрезе серо-красного цвета. В 1-й сегменте расширенные бронхи за полнены слизисто-гнойпыми массами. Линии пересечения бронха на ходятся на расстоянии 3 и 1,5 см от края опухоли. Слизистая оболочка резецированных отрезков главного и нижнедолевого бронхов не изме нена. На разрезе просвет верхнедолевого бронха обтурирован плотной опухолью, частично выступающей в просвет главного бронха. Опухоль образует неправильной формы узел размером 3,5x2x2,5 см, который прорастает долевой бронх и распространяется в легочную ткань. Ле гочная артерия на протяжении 1 см интимно сращена с опухолью.
Гистологическое исследование препарата: недифференцированный мелкоклеточный рак. В лимфатических узлах массивные метастазы ра ка того же строения. В крае сечения бронха элементов опухоли не об наружено. В легочной ткани фиброатслектаз, ретенционные бронхоэктазы, хроническая интерстициальная пневмония.
Послеоперационный период осложнился ателектазом доли на сто роне операции. Применялись лечебные бронхоскопии с аспирацией
вязкой мокроты. В остальном послеоперационное течение без ослож
Через 1"/2 месяца после операции бронхиальный анастомоз в хоро шем состоянии. При ангиопульмонографии сосуды нижней доли лево го легкого хорошо контрастируются (рис. 75).
Основным противопоказанием к лобэктомии и пластике -бронхов при верхнедолевом бронхолегочном раке является большая распространенность процесса. В каждом конкретном случае противопоказания к пластике бронхов следует оценивать сугубо индивидуально. Мы их несколько суживаем при опера циях у пожилых людей с низкими функциональными резерва ми, особенно при правостороннем раке. У этой категории боль ных «компромиссная» лобэктомия с резекцией и пластикой бронхов часто предпочтительнее, чем более опасная для жиз ни и обычно инвалидизирующая пульмовэктомия.
ПРОЧИЕ ПОКАЗАНИЯ
Необходимость резекции и пластики может возникнуть при воспалительном сужении бронхов, полипозном эндобронхите и нагноившихся бронхогенных кистах прикорневой локализации.
Сужение бронхов вследствие неспецифического воспали тельного процесса встречается редко. Narkiewicz et al. (1964) описали 3 больных, оперированных по поводу неспецифиче ского ограниченного эндобронхита. В дифференциальном ди агнозе следует учитывать сифилис, бронхолегочные опухоли, туберкулез и инородные тела бронха.
Объем хирургического вмешательства при воспалительном стенозе зависит от степени изменений и состояния легочной паренхимы. Иногда бывает достаточно удалить грануляцион ную ткань из просвета бронха или иссечь рубцовые перибронхиальные тяжи. При ограниченном поражении показана сег ментарная либо клиновидная резекция бронха.
Мы наблюдали 2 больных с хроническим нагноением верх ней доли правого легкого и сужением долевого бронха, обу словленным неспецифическим воспалительным процессом. У одной больной хроническая неспецифическая пневмония с бронхоэктазами была следствием полипозного эндобронхита среднедолевого бронха. Этим 3 больным произведено удаление доли с клиновидной резекцией главного бронха.
В одном случае показания к резекции правого главного бронха возникли при нагноившейся бронхогенной кисте верх ней доли. Типичную лобэктомию выполнить не удалось, так как утолщенная стенка кисты была плотно сращена с доле вым и главным бронхами. Сделано удаление верхней доли с клиновидной резекцией главного бронха.
Г Л А В А I V
МЕТОДИКА И ТЕХНИКА ОПЕРАЦИЙ
АНЕСТЕЗИЯ
Все пластические операции на крупных бронхах необходи мо выполнять под наркозом с управляемым дыханием.
Главной особенностью наркоза при резекции и пластике бронхов является необходимость обеспечения достаточной ле гочной вентиляции при длительном зиянии просвета трахеи или пересеченного крупного бронха (Т. Т. Богдан, 1955;
В. С. Северов, 10. Н. Жилин, А. П. Давыдов, 1961; Ф. Ф. Амиров, 1962; О. М. Авилова, Е. П. Кравченко, 1964; Л. К. Богуш,
В. С. Северов, Ю. Н. Жилин, В. Ф. Диденко, 1965; О. Д. Колюцкая, В. С. Трусов, В. Н. Цибуляк, 1965, и др.). Следует также иметь в виду, что пластические операции на бронхах часто выполняют у больных пожилого возраста со значитель ными изменениями со стороны дыхательной и сердечно-сосу дистой системы и низкими функциональными резервами.
Перед операцией анестезиолог должен детально ознако миться с характером патологического процесса на основании рентгенологических и бронхологических данных, а затем обсу дить с хирургом план предстоящего вмешательства и возмож ные варианты резекции и реконструкции трахеобронхиального дерева.
В операционной необходимо иметь набор стерильных интубационных трубок для различных способов эндотрахеальной и эндобронхиалыюй интубации, а также последовательной реинтубации в ходе наркоза. При вероятной потребности в проб ном раздувании ателектазированного легкого после разрыва бронха нужно подготовить второй наркозный аппарат со сте рильными интубационными и соединительными трубками.
8 Заказ 255 |
Они нужны также для интубации пересеченного бронха со стороны плевральной полости в случаях возможной необходи мости резекции бифуркации трахеи.
В процессе обследования и подготовки к операции больным при сопутствующих заболеваниях назначают необходимую те рапию. Возбужденным больным с лабильной психикой за 2- 3 дня до операции мы назначали андаксин или мекратон по 200 мг 2-3 раза в день. Глюкокортикоиды, как правило, не назначали из-за их возможного отрицательного влияния на процесс регенерации.
Ведение наркоза осуществлялось по следующей методике-
200 мг промедола и 1 мг атропина. Введение в наркоз прово дят вдыханием через маску фторотапа с закисью азота и кис лородом при одновременной внутривенной инъекции барбиту ратов или стероидных наркотиков. Для проведения интубации применяют деполяризующие миорелаксанты.
С целью обеспечения адекватной вентиляции легких на время широкого вскрытия трахеи и бронхов можно использо вать различные приемы. В эксперименте на животных мы сравнивали эффективность ряда из них. Пересекаемый бронх закрывали зажимом или марлевым тупфером со стороны ра ны, использовали бронхоблокаторы, эндобронхиальную инту бацию однопросветными и двупросветными трубками, чресплевральную интубацию с выключением одного легкого и шунт-дыханием. В результате экспериментальных исследова ний и главным образом клинического опыта мы при всех пла стических операциях на бронхах считаем наиболее рациональ ным способ эндобронхиальной интубации. Этот способ позво ляет обеспечить полноценную вентиляцию здорового легкогопосле пересечения бронха на стороне операции, исключает затекание мокроты, гноя и крови в вентилируемое легкое,.
Предотвращает обтурацию дыхательных путей кусочками тка ни опухоли и создает оптимальные условия для оперирующего хирурга.
В клинической практике при операциях на правом главном
бронхе нужно ввести в правый бронх либо обычную однопросветную трубку, либо трубку Гордон-Грина. Еще более удобна
дувной манжеткой (рис. 76). Эта трубка изготовлена в Инсти-

Рис. 76. Двупросвотная трубка с узкой надувной манжеткой.
А- схема конструкции трубки; Б - проводник для интубации; В - положение трубки в правом и левом бронхах.
туте резиновых и латексных изделии и успешно применена более чем при 40 различных операциях на легких и бронхах.
Выбор метода интубации зависит не только от стороны по ражения, но и от особенностей патологического процесса и ха рактера оперативного вмешательства. Поэтому в ходе опера ции иногда приходится реинтубировать больного.
Схематическое изображение основных вариантов интуба ции при типичных пластических операциях на крупных брон хах представлено на рис. 77.
В качестве основных наркотических веществ можно при менять эфир, эфир с закисью азота, фторотан, фторотан с за кисью азота, хлороформ или трилен с закисью азота. Их при менение на нашем материале показано в табл. 18.
ТАБЛИЦА 18 |
||||||||||
Применение |
различных основных |
наркотических |
||||||||
пластических |
операциях |
на бронхах |
||||||||
Посттравматиче |
||||||||||
окклюзия |
||||||||||
Туберкулезное по |
||||||||||
ражение бронха |
||||||||||
Посттуберкулез |
||||||||||
бронхостеноз |
||||||||||
Доброкачествен |
||||||||||
опухоли брон |
||||||||||
И т о г о. . . |
||||||||||
В течение последнего времени в качестве основных нарко тических веществ при пластических операциях на бронхах наши анестезиологи применяют фторотан или хлороформ. Эти анестетики по сравнению с эфиром и закисью азота имеют су щественные преимущества. Газово-наркотическая смесь с фторотаном или хлороформом обладает сильными наркотическими свойствами, не раздражает слизистой оболочки дыхательных путей, безопасна в отношении взрыва и позволяет создавать любую концентрацию кислорода, что особенно важно во время длительного выключения из вентиляции одного легкого.

Рис. 77. Схема основных вариантов интубации при пластических операциях на крупных бронхах.
Фторотан и хлороформ применяют по общепринятой мето дике через «фторотек» конструкции ВНИИМИиО или «флюотек Марк-П», помещенный вне блока циркуляции газов.
При поддержании основного наркоза по полузакрытому контуру концентрация наркотика во вдыхаемой смеси не пре вышает 1,5 об.% при потоке кислорода до 5Л /М инМетодом вы бора можно считать поддержание наркоза газово-наркотиче- ской смесью, состоящей из 0,5 об. % фторотана в потоке заки си азота с кислородом в соотношении 2:1, 1:1.
Искусственную вентиляцию легких проводят автоматиче ским респиратором АНД-2 на фоне длительного апноэ, вызван ного введением миорелаксантов антидеполяризующего типа, в
режиме умеренной гипервентиляции |
не ниже 28 мм |
||
Из главного бронха оперируемой стороны |
через катетер, |
||
введенный в соответствующий канал |
интубационной |
||
ки, постоянно или периодически отсасывают |
|||
В случаях длительного выключения |
из вентиляции |
||
няющего воздушность легкого может развиться так называе мая спленизация. Она происходит вследствие пропотевания жидкости и даже форменных элементов крови из легочных капилляров в альвеолы. С целью предупреждения спленизации выключение легкого из вентиляции на оперируемой сто роне следует производить только после разделения всех плевральных сращений. Такая методика позволяет также пред упредить гипоксию вследствие большого сброса неоксигенированной крови в левое предсердие. После полного спадения легкого кровоток в нем резко уменьшается и артерио-венозный шунт менее выражен.
На период наложения бронхиального анастомоза желатель но проводить вентиляцию легкого не автоматическим, а руч ным способом, сообразуясь с манипуляциями хирурга и мак симально облегчая их.
Значительная продолжительность оперативного вмешатель ства и сложность обезболивания на некоторых этапах обуслов ливают необходимость постоянного электрокардиографическо го и энцефалографического контроля. У наиболее тяжелых больных приходится также исследовать кислотно-щелочное состояние и объем циркулирующей крови.
После зашивания раны грудной стенки делают бронхоско пию для контроля анастомоза и тщательного туалета бронхи ального дерева. Тубус дыхательного бронхоскопа извлекают после снятия остаточной кураризации и восстановления адек ватного спонтанного дыхания.
Пример течения наркоза при лобэктомии с резекцией глав ного бронха приведен на рис. 78.

Рис. 78. Больной К., 55 лет. Верхняя лобэктомия справа с циркулярной резекцией главного бронха. Основной наркоз - хлороформ в потоке закиси азота.
Карта анестезиолога. Однолегочная вентиляция 3 часа 10 минут.
Необходимости шунт-дыхания, которое осуществляют через интубационную трубку, введенную в периферический конец пересеченного бронха со стороны вскрытой плевральной поло сти, на нашем материале не возникало.
Осложнений, связанных с анестезией, во время наркоза и в раннем послеоперационном периоде не отмечалось.
ОПЕРАТИВНЫЙ ДОСТУП
Большинство пластических операций на бронхах сочета ется с различными вариантами резекции легких. Иногда по ходу вмешательства возникает также необходимость краевой или циркулярной резекции легочной артерии с наложением бокового шва или межартериального анастомоза конец в ко нец или бок в конец. Поэтому применяемый доступ должен обеспечить выполнение легочной операции при достаточно сво бодном поле для манипуляций в области трахеобронхиального угла, деления главных бронхов и расположения крупных ле гочных сосудов. Перечисленным требованиям в наибольшей степени удовлетворяет стандартная боковая торакотомия по пятому межреберью в положении больного на здоровом боку.
Стандартная боковая торакотомия дает возможность сво бодно выполнить необходимые манипуляции во всех отделах плевральной полости, обеспечивает удобный подход к области трахеобронхиального угла, ко всем элементам корня легкого и к главной междолевой щели. При этом доступе имеется пол ная возможность пластической операции на бронхах и ниж нем отделе трахеи с одновременным удалением пораженной части легкого. Можно также сочетать восстановительную опе рацию на бронхах с краевой или циркулярной резекцией ле гочной артерии.
У некоторых больных, однако, лучше применять не боко вой, а задний доступ в положении на животе с вскрытием плев
Мы считаем прямым показанием к заднему доступу вос становительную операцию после травматического разрыва бронха. Опыт показывает, что сзади в этих случаях значитель но облегчается выделение главного бронха из рубцово изме ненных тканей средостения и уменьшается опасность повреж дения магистральных сосудов коллабированного легкого.
Вторым прямым показанием к заднему доступу является операция по поводу доброкачественной опухоли, которая ло кализуется в устье главного бронха. При этом всегда возни-
Бронхоскопические оперативные вмешательства - это настоящие хирургические операции, чреватые осложнениями и неблагоприятными последствиями.
Кровотечение в просвет дыхательных путей - одно из наиболее реальных и опасных осложнений. Кровотечение чаще возникает при удалении сильно васкуляризованных доброкачественных и злокачественных опухолей трахеи и бронхов.
Причиной, как правило, бывает механическое повреждение сосудов опухоли тубусом бронхоскопа или инструментом. Но и при использовании электрокоагуляционной петли и лазерного излучения недостаточная коагуляция сосудов может осложниться кровотечением. Наиболее опасно кровотечение при выполнении операции под местной анестезией с применением бронхофиброскопа или видеоскопа. Кровь мгновенно закрывает объектив, и видимость полностью исчезает, а через узкий инструментальный канал невозможно удалить интенсивно изливающуюся кровь и образующиеся сгустки. Больной при этом может быстро потерять сознание и задохнуться, «утонув» в собственной крови. Это обстоятельство заставляет большинство бронхологов критически относиться к местной анестезии и гибким эндоскопам при выполнении эндоскопических вмешательств на бронхах и применять их лишь в редких случаях, по очень узким показаниям и при наличии веских противопоказаний к общему обезболиванию. Но и при выполнении бронхоскопической операции под общей анестезией начавшееся кровотечение даже средней интенсивности значительно затрудняет продолжение вмешательства, ухудшая видимость и делая практически невозможным использование лазера. Профилактикой кровотечения является тщательная коагуляция поверхности опухоли или области стеноза перед началом резекции.
К сожалению, заранее предсказать риск развития кровотечения можно далеко не во всех случаях, поэтому к нему нужно быть готовым всегда: иметь мощный электроотсос, запас тупферов для прижатия места кровотечения, ленту из гемостатической марли для тампонирования бронха, гемостатические растворы (е-аминокапроновая кислота, трансамча, дицинон).
При состоявшемся кровотечении , с которым удалось справиться, не следует забывать о важности тщательной аспирации из мелких бронхов, излившейся в них крови, для чего перед экстубацией необходимо выполнить санационную бронхо-фиброскопию и промывание бронхов.
Перфорация стенки трахеи или бронха.
Возникновение этого осложнения наиболее реально во время лазерной реканализации трахеи при ее рубцовом или опухолевом стенозе, а также при эвапорации опухоли с преимущественно эндофитным ростом, не имеющей четких границ. Стенку трахеи или бронха можно прожечь , если отклониться от оси просвета дыхательной трубки и углубиться в ткань рубца или опухоли в неверном направлении. Наиболее опасна перфорация стенки в тех зонах, где непосредственно к трахее или бронху примыкает пищевод или крупный кровеносный сосуд. Сквозное ранение в этом месте может осложниться развитием трахеопищеводного свища или фатальным кровотечением. Поэтому не рекомендуется производить глубокую эвапорацию опухолевой ткани в области мембранозной стенки трахеи или крупного бронха или захватывать в коагуляционную петлю мембранозную стенку трахеи при удалении исходящей из нее опухоль». Нужно быть также предельно внимательным при лазерной резекции опухолей, растущих из латеральной стенки левого главного бронха или расположенных в области шпоры правого главного бронха.
Неукоснительное соблюдение основных правил применения лазерной или электрохирургической техники является залогом безопасного выполнения эндоскопических операций.
Повредить мембранозную стенку трахеи или главного бронха можно и при попытке бужирования рубцового стеноза тубусом жесткого бронхоскопа без предварительного рассечения его лазером, так как именно мембранозная стенка трахеи является ее самым слабым местом. Даже небольшой разрыв стенки крупного бронха может осложниться развитием медиастинальной эмфиземы или пневмоторакса, нередко напряженного.
Этому способствуют инжекционная ИВЛ и кашель во время пробуждения больного и в послеоперационном периоде. Как правило, при этом в области шеи и передней грудной стенки возникает подкожная эмфизема, выявляемая по характерной крепитации.
Сквозные ранения трахеи и пищевода , а также повреждения стенок дыхательных путей, сопровождающиеся нарастающей эмфиземой средостения, требуют экстренной торакотомии и ушивания дефекта. Наряду с этим ограниченные дефекты стенки трахеи без повреждения пищевода могут зажить самостоятельно, если на время закрыть их эндотрахеальным стентом и назначить большие дозы антибиотиков, в чем мы неоднократно имели возможность убедиться.
Воспламенение световода в просвете дыхательных путей может иметь очень тяжелые последствия. Это может произойти, если использовать световоды без воздушного или газового охлаждения.
Во время бронхоскопии под общим обезболиванием с ИВЛ в просвете трахеи и бронхов создается повышенная концентрация кислорода. В насыщенной кислородом атмосфере синтетическая оболочка световода может воспламениться, что обусловливает тяжелый ожог слизистой оболочки дыхательных путей. Это также может случиться, если луч лазера попадет на введенный в трахею предмет, изготовленный из горючего материала: интубационную трубку, трахеотомическую канюлю, эндотрахеальный стент, катетер для инжекционной ИВЛ, инородное тело органического происхождения.
Приводим наблюдение.
Больной Г., 26 лет, житель Северной Осетии, во время застолья поперхнулся куском мяса и стал задыхаться. Кто-то из друзей попытался протолкнуть застрявший в гортаноглотке кусок в пищевод с помощью первой попавшейся под руку деревянной щепки. Больному удалось проглотить мясо, однако после этого у него возник постоянный кашель, а через 2 нед присоединилось стридорозное дыхание.
При ларингоскопии в подскладочном пространстве обнаружены утолщение стенки и сужение просвета трахеи, в связи с чем больной был направлен во Всероссийский онкологический научный центр (ВОНЦ) им. Н. Н. Блохина РАМН. Патология была расценена как опухоль трахеи, и было решено выполнить ее лазерную резекцию. Во время эвапорации «опухоли», производимой под общим обезболиванием с ИВЛ кислородом, произошло воспламенение фрагмента деревянной щепки, вонзившейся в стенку трахеи непосредственно под связками и вызвавшей выраженную пролиферативную реакцию, принятую за опухоль. Последовал тяжелый ожог слизистой оболочки трахеи, вызвавший развитие нескольких рубцовых стенозов на протяжении всей трахеи, наиболее значительный из которых, протяженностью около 5 см, локализовался в нижней половине грудной части трахеи.
Для дальнейшего лечения в ноябре 1997 г. больной переведен в нашу клинику с выраженным стридорозным дыханием и дыхательной недостаточностью. Выполнена лазерная реканализация трахеи, в области нижней стриктуры установлен эндотрахеальный стент Дюмона длиной 6 см, после чего больной в удовлетворительном состоянии был выписан. Циркулярная трахеальная резекция была расценена как невыполнимая в связи со множественным характером стриктур и обширностью поражения трахеи. В последующие 3 года больной был трижды госпитализирован для замены эндопротеза и удаления грануляций (рис. 1). Протяженность стенозов с каждым разом увеличивалась. Обсуждалась возможность установления бифуркационного динамического стента Фрайтага. В сентябре 2000 г. в связи с очередным ухудшением дыхания и экспекторации больной намеревался приехать в клинику, однако в начале октября у него внезапно развился приступ удушья, приведший к смерти.
Профилактикой подобных осложнений является обязательное охлаждение конца световода воздухом или сжатым инертным газом. Мы используем для этого обычный компрессор, а в последние годы - углекислый газ, баллон с которым установлен в кабинете бронхоскопии. Газ под давлением 1 - 1,5 нагнетается в пластиковый чехол световода у его проксимального конца. Благодаря этому, выполнив большое число лазерных операций в условиях общего обезболивания с инжекционной ИВЛ кислородом, мы избежали воспламенения световода в просвете дыхательных путей. Единственный случай произошел при апробации гольмиевого ИАГ-лазера, световоды которого не были оборудованы системой газового охлаждения. Поэтому, как показывает наш опыт, при адекватной продувке оболочки световода опасность ее воспламенения невелика даже при выполнении операции под общим обезболиванием с ИВЛ.
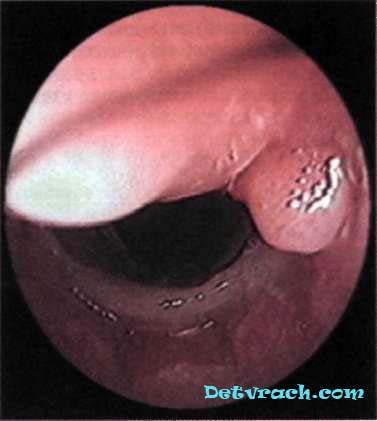
Рис. 1. Бронхоскопия больного Г., 26 лет, с Рубцовым стенозом трахеи после ее термического ожога. Грануляции у проксимального конца эндотрахеального стента.
Тем не менее, мы считаем целесообразным включать лазерное излучение только на фоне апноэ, что уменьшает концентрацию кислорода в просвете дыхательных путей в момент эвапорации и к тому же делает объект неподвижным. Кроме того, мы категорически не рекомендуем применять лазерное излучение при наличии в просвете дыхательных путей трубок, стентов, катетеров и т. д., например удалять лазером грануляции у концов стента.
Газ или воздух, проходящий внутри оболочки световода, сдувает дым и частички обугленной ткани с его конца. При этом улучшается видимость во время операции и меньше подгорают концы световодов. Следует заметить, что использование углекислого газа для охлаждения световодов при выполнении бронхофиброскопии под местной анестезией вызывает у больных неудержимый кашель. В таких случаях единственно возможной является продувка световодов атмосферным воздухом с помощью компрессора.
Еще одно осложнение связано с использованием бронхо-фиброскопа в качестве проводника для лазерного световода. При значительном изгибе дистального конца бронхофиброскопа вместе с проведенным по его каналу световодом во время лазерной эвапорации опухоли верхнедолевого бронха внезапно прогорела оболочка световода в области максимального изгиба и был так сильно поврежден тубус бронхофиброскопа, что потребовалась его полная замена. С тех пор мы стараемся как можно реже использовать бронхофиброскопы при лазерных операциях и тщательно контролируем степень изгиба световода.
Анестезиологические осложнения, возникающие во время бронхоскопических оперативных вмешательств, мало чем отличаются от таковых при диагностических и лечебных бронхоскопиях и подробно описаны нами ранее.
Необходимо еще раз отметить, что эндоскопические операции на трахее, как правило, сопровождаются более значительной травмой и требуют добавления местной анестезии в оперируемой области. Без этого возрастает частота ларингоспазма и мучительного кашля в момент пробуждения больного и в послеоперационном периоде.
4278 0
Показаниями к эндоскопическим операциям являются опухоли и рубцовые стенозы трахеи и крупных бронхов. Это положение нуждается в уточнениях. В первую очередь патологические изменения должны быть доступны для жесткого бронхоскопа, т. е. локализоваться в трахее, главных, промежуточном и долевых бронхах. При более глубоком расположении опухоли выполнение операции в ряде случаев возможно, но требует применения бронхофиброскопа и сопряжено с определенными техническими трудностями.
Эндоскопические операции на трахее и бронхах ни в коем случае не следует противопоставлять классическим открытым операциям, возможности и радикальность которых неизмеримо выше. Однако в связи со значительно меньшей травматичностью эндотрахеальные и эндобронхиальные операции имеют преимущества в следующих конкретных ситуациях.
Эндоскопические операции показаны при экзофитно растущих доброкачественных опухолях трахеи и крупных бронхов, когда их удаление с помощью электрокоагуляционнои петли или лазера является достаточно радикальным. Это в первую очередь относится к одиночным папилломам, при которых после технически правильно выполненного удаления обычно наступает выздоровление. Эндоскопическим способом могут быть радикально удалены довольно редко встречающиеся эндобронхиальные полипы и опухоли неэпителиального происхождения: фибромы, липомы, фибролипомы и т. д.
При множественных папилломах гортани, трахеи и крупных бронхов, склонных к рецидивам, эндоскопические операции, хотя и не являются радикальными, но могут считаться методом выбора, так как классические открытые операции, как правило, противопоказаны.
Эндоскопические операции могут быть выполнены при относительно редких экзофитно растущих и имеющих хорошо сформированную ножку так называемых типичных карциноидах трахеи и крупных бронхов. При комбинированном (в том числе интрамуральном) росте опухоли эндоскопическая операция может быть оправдана лишь в качестве первого этапа лечения при наличии осложнений или у ослабленных пациентов преклонного возраста, у которых радикальная операция представляет чрезмерный риск.
Эндоскопическая операция может быть использована в качестве паллиативного вмешательства при злокачественных опухолях трахеи и главных бронхов в следующих случаях:
- При нерезектабельных злокачественных опухолях, вызывающих нарушение проходимости трахеи и крупных бронхов с симптомами гипоксии, постстенотической инфекции, массивного кровохарканья, неукротимого кашля. В этой ситуации эндоскопическая реканализация трахеи или главного бронха с последующим введением стента позволяет вывести больного из критического состояния, устранить асфиксию и продлить жизнь больного, улучшив качество его жизни, а также дает возможность в более безопасных условиях провести курс лучевой или химиотерапии.
- При резектабельных злокачественных опухолях главных или долевых бронхов, когда тяжесть состояния больного, обусловленная выраженными вентиляционными нарушениями, постстенотической пневмонией или нагноением в обтурированных отделах легкого, не позволяет выполнить радикальную операцию. В этих случаях удаление экзофитной части опухоли, восстанавливая дренаж и вентиляцию, позволяет уменьшить интоксикацию и гипоксию, улучшить состояние больного и подготовить его к операции.
- При резектабельных злокачественных опухолях крупных бронхов у лиц преклонного возраста или больных с тяжелой соматической патологией, состояние которых делает риск радикальной операции крайне высоким, а также в случае категорического отказа больного от радикальной операции.
Показанием к эндоскопическому хирургическому вмешательству служат также грануляционные и рубцовые стенозы трахеи и главных бронхов, возникающие после трахеостомии или длительной интубации трахеи, а также (редко) после резекций и пластических операций на трахее и крупных бронхах. Эндоскопическая операция при этой патологии показана в следующих случаях:
- При наличии единичных грануляций, нередко возникающих в трахее в области трахеостомы или у конца трахеостомической канюли. При этом лазерная эвапорация может быть вполне успешной и привести к выздоровлению.
- При декомпенсированных Рубцовых стенозах трахеи, сопровождающихся выраженной дыхательной недостаточностью и/или гнойным трахеобронхитом, делающим риск радикальной операции чрезмерно высоким. В большинстве подобных случаев бронхоскопическую реканализацию трахеи выполняют в экстренном или неотложном порядке по жизненным показаниям и она является этапом подготовки больных к циркулярной резекции стенозированного участка трахеи.
- При декомпенсированных Рубцовых стенозах трахеи у больных, состояние которых требует продолжительного лечения или реабилитации и не позволяет прибегнуть к радикальному оперативному вмешательству (пациенты с неврологическими последствиями тяжелой черепно-мозговой травмы, гнойными осложнениями комбинированных травм или внутриполостных оперативных вмешательств, истощенные больные с аспирационной пневмонией при сочетании стенозов с трахеопищеводными свищами или дефектами).
- При декомпенсированных или субкомпенсированных Рубцовых стенозах трахеи большой протяженности (более 8— 9 см), наличии нескольких стенозов или участков трахеомаляции на разных уровнях трахеи, а также рецидивирующих стенозов после перенесенных ранее хирургических вмешательств на трахее, делающих ее мобилизацию и резекцию практически невозможной.
При операциях на органах грудной клетки принципиально важно применение такого вида анестезии, который позволил бы предупредить патофизиологические изменения в организме, связанные со специфическими особенностями внутригрудных операций (открытый пневмоторакс, коллапс легкого, парадоксальное дыхание, флотация средостения, нарушение вентиляционно-перфузионного соотношения, уменьшение венозного возврата крови, сердечного выброса, патологические рефлексы при раздражении обширных шокогенных зон, кровопотеря). Этим требованиям отвечает комбинированная (многокомпонентная) анестезия.
У больных с заболеваниями легких еще до операции имеются нарушения газообмена, гемодинамики, функции печени, почек, обмена веществ, обусловленные воспалительным, туберкулезным или опухолевым процессом и выключением части легочной ткани из акта дыхания. Из специальных методов исследования в хирургии легких особое место занимают общее и раздельное определение легочных функций (показатели легочных объемов, вентиляционной, механической функций, диффузионной способности, вентиляционно-перфузионного соотношения, газового состава крови, КЩС).
Предварительная подготовка направлена на устранение обострения воспалительного процесса, перифокального воспаления, уменьшение гнойной интоксикации, улучшение функций дыхания, кровообращения, печени, почек, коррекцию нарушений обмена (белкового, электролитного, витаминного), КЩС, волемических сдвигов. У больных с избыточной легочно-бронхиальной секрецией, выделением большого количества мокроты, бронхоспастическими реакциями большое значение имеет восстановление проходимости дыхательных путей: постуральный дренаж, лечебная бронхоскопия, предусматривающие удаление содержимого бронхиального дерева и последующее введение антибиотиков, протеолитических ферментов, бронхолитических средств. «Осушение» трахеобронхиального дерева имеет большое значение в профилактике осложнений как во время операции (асфиксия, ателектаз), так и в послеоперационном периоде (пневмония).
Премедикания включает транквилизаторы, анальгетики, ваголитические и антигистаминные препараты, создающие оптимальный фон для анестезии. Обычно на ночь назначают снотворное из группы барбитуратов и транквилизатор. В день операции, за 2 ч до ее начала, больному назначают транквилизатор (седуксен, элениум, триоксазин, мепробамат). За 40 - 50 мин до анестезии в/м или п/к (в экстренных ситуациях в/в на операционном столе) вводят 10 - 20 мг промедола, 0,5-1 мг атропина, 5 - 10 мг седуксена или атропин в сочетании с препаратами для НЛА (0,05 - 0,1 мг фентанила, 2,5 - 5 мг дропери-дола), назначают антигистаминные препараты. Седуксен и дроперидол уменьшают сопротивление в сосудах малого круга кровообращения, и поэтому рекомендуются больным с легочной гипертензией. У больных с заболеваниями легких следует избегать выраженного нейровегетативного торможения, чтобы предупредить длительное угнетение кашлевого рефлекса и замедленное восстановление самостоятельного дыхания в конце операции. Показания к применению препаратов для введения в анестезию при операциях на легких существенно не отличаются от общих положений. При операциях на легких широко распространены для введения в анестезию производные барбитуровой кислоты. Преимущество имеет гексенал, не содержащий серы и поэтому менее способный вызывать спастические реакции (ларингоспазм, бронхоспазм). Для уменьшения дозы барбитуратов, быстрого угнетения кашлевого рефлекса, бронхоспастических реакций применяют также комбинированное введение в наркоз путем сочетания препаратов для внутривенного наркоза с ингаляцией фторотаном, закисью азота и др.
Интубация - один из наиболее ответственных этапов комбинированной анестезии при операциях на легких. При выборе метода интубации важно учитывать, чтобы он обеспечил: оптимальные условия для поддержания адекватного газообмена при различных операциях, в том числе и сопровождающихся нарушением герметичности дыхательных путей; надежную защиту здоровых отделов легких от попадания в них патологического содержимого из пораженных частей; аспирацию содержимого бронхиального дерева одного легкого без прекращения вентиляции другого; полное или частичное выключение оперируемого легкого из вентиляции, быструю смену вида вентиляции (однолегочная, двулегочная); оптимальные условия для технического выполнения операции (неподвижное, малоподвижное легкое), безопасность и техническую легкость выполнения.
В зависимости от индивидуальных особенностей больного, характера основного патологического процесса, сопутствующих заболеваний, объема и вида операции применяют следующие способы интубации: эндотрахеальную интубацию (иногда в сочетании с положением для постурального дренажа); эндотрахеальную интубацию в сочетании с тампонадой бронхов пораженных отделов легкого или блокадой их специальными блокаторами; эндобронхиальную интубацию здорового легкого; раздельную интубацию главных бронхов обоих легких. Эндотрахеальная интубация имеет ряд серьезных недостатков в хирургии легких: не изолирует пораженное легкое от интактного, не создает условий для адекватной ИВЛ при нарушении герметичности дыхательных путей, для полного или частичного выключения пораженного легкого из вентиляции. Поэтому показания к ней ограничены и включают: малотравматичные операции, не сопровождающиеся нарушением герметичности дыхательных путей и выделением большого количества мокроты (удаление поверхностно расположенных опухолей, кист легкого, краевая резекция); изменения анатомии и топографии верхних дыхательных путей из-за патологического процесса (сужение голосовой щели, искривление, смещение трахеи и т. д.), затрудняющие выполнение других видов интубации или блокады бронхов; резкое снижение функциональных резервов внешнего дыхания больного, когда даже небольшое повышение сопротивления в дыхательных путях (напртмер, в случае применения двухпросветной трубки) резко ухудшает условия вентиляции легких.
Тампонада и блокада бронхов при эндотрахеальной интубации применяется для защиты здоровых отделов легкого при операциях, сопровождающихся выделением большого количества мокроты, и при операциях, выполняемых на высоте легочного кровотечения и при наличии бронхиальных свищей. При правильном выполнении тампонада и блокада бронхов защищают здоровые отделы легких от попадания в них патологического содержимого во время операции и создают условия для адекватной ИВЛ при меньшем сопротивлении в дыхательных путях по сравнению с некоторыми другими способами (интубация двухпросветными трубками).
Для выполнения тампонады или блокады бронхов необходимо иметь, кроме обычных принадлежностей для интубации, дыхательный бронхоскоп, набор различных бронхоблокаторов, проводников, вакуум-аппарат с катетерами. Тампонаду бронхов осуществляют с помощью марлевых тампонов из узких полосок различной длины. Тампон вводят через бронхоскоп с помощью металлического проводника, имеющего вид стержня или полой трубочки. П. А. Куприянов, М. С. Григорьев, М. Н. Аничков (1948, 1949) сконструировали специальный бронхоскоп с боковой прорезью, облегчающей выполнение тампонады как главных, так и долевых бронхов.
Для выполнения блокады бронхов предложены различные блокаторы, большинство из которых представляет собой модификациюблокатора Мэгилла. Од имеет вид длинной резиновой трубки с раздувной манжеткой на дистальном конце. Блокатором Мэгилла можно блокировать как главные, так и долевые бронхи. Более надежны, так как они прочнее фиксируются в бронхе, комбинированные бронхиальные блокаторы - соединение бронхоблокатора и эндотрахеальной трубки (бронхоблокатор Штюрцбехера). Для блокады правого верхнедолевого бронха предложена специальная трубка Вехтакота (1954), для блокады левого бронха применяется бронхоблокатор Макинтоша - Литердела. Выгодно отличается от ранее предложенных двухпросветный обтуратор В. И. Сипченко. Металлическая трубка, идушая внутри обтуратора, позволяет им управлять и облегчает выполнение блокады. Кроме того, через внутренний просвет обтуратора можно постоянно отсасывать секрет бронхов, накапливающийся дистальнее манжетки.
Методы тампонады и блокады бронхов имеют недостатки, из-за которых их применение ограничено: выключение из вентиляции легкого или доли сопровождается нарушением вентиляционно-перфузионного соотношения, развитием эффекта шунта - сброса неоксигенированной крови из системы легочной артерии в большой круг кровообращения; при тампонаде и блокаде бронхов трудно создать необходимую степень коллабирвания легкого или доли, что затрудняет техническое выполнение отдельных этапов операции; из-за отсутствия надежных методов фиксации бронхоблокаторов возникает опасность их смещения, инфицирования здоровых отделов легких, затруднения адекватной ИВЛ.
Смещение блокаторов может произойти в момент укладывания больного в операционное положение, при манипуляциях хирурга. Оно чаще наблюдается при блокаде правого главного бронха из-за небольшой его длины. Выполнение тампонады и блокады бронхов, особенно долевых, требует определенных технических навыков и нередко бронхоскопического и рентгенологического контроля. Для профилактики осложнений необходимы постоянный контроль положения тампона и блокатора, тщательная аспирация содержимого трахеобронхиального дерева.
Эндобронхиальная интубация здорового легкого - менее сложный метод по сравнению с тампонадой и блокадой бронхов. Однако однолегочная вентиляция сопровождается ателектазом легкого на стороне операции и эффектом шунта, приводящим к гипоксемии. При интубации главного бронха существует опасность перекрытия устья верхнедолевого бронха, особенно справа. При удалении доли легкого в остающейся легочной ткани вследствие длительного ателектаза возникают глубокие патоморфологические изменения вплоть до спленизации, неблагоприятно влияющие на течение послеоперационного периода. В культе главного бронха удаляемого легкого при однолегочной интубации скапливается содержимое (кровь, гной), которое при экстубации может попасть в главный бронх здорового легкого и даже вызвать асфиксию. Во избежание этого осложнения необходима тщательная санация бронха через интубационную трубку, иногда прибегают к открытой обработке культи бронха с предварительным отсасыванием бронхиального содержимого. Показания к эндобронхиальной интубации здорового легкого ограничены и включают: пульмонэктомию при тотальном поражении удаляемого легкого с полным выключением его функции до операции; операции, сопровождающиеся нарушением герметизма в дыхательных путях (операции по поводу бронхиальных свищей, реконструктивные операции на трахее и бронхах).
Для интубации правого бронха наиболее широко применяется трубка Гордона - Грина (можно использовать и обычную интубационную трубку небольшого диаметра со срезом справа во избежание перекрытия верхнедолевого бронха), для интубации левого бронха - трубка Макинтоша - Литердела (1955). В 1957 г. во ВНИИР была создана трубка для правого бронха, позволяющая осуществлять вентиляцию правого легкого при одновременном выключении левого.
При однолегочной вентиляции особое внимание следует уделять установлению и фиксации трубки в правильном положении, чтобы предотвратить осложнения, связанные со смещением и перегибами трубки.
Раздельная интубация главных бронхов в последние годы получила наиболее широкое распространение, так как по сравнению с другими имеет ряд преимуществ: наиболее полно отвечает требованиям, предъявляемым к интубации в хирургии легких. Показания к применению интубации двухпросветными трубками: необходимость защиты здорового легкого от попадания инфицированного материала при патологических процессах с выделением большого количества мокроты; операции на высоте легочного кровотечения; необходимость герметизации дыхательных путей при бронхиальных свищах; реконструктивные операции на трахее и бронхах; профилактика имплантационных метастазов при операциях по поводу рака; создание максимальных удобств для выполнения операции.
Для проведения анестезии с раздельной интубацией главных бронхов необходим набор специальных двухпросветных трубок и соединительных элементов к наркозному аппарату. В клинической практике получили наибольшее распространение трубки Гебауэра и Карленса. Успех раздельной интубации бронхов определяется правильным выбором гипа и размера трубки в зависимости от индивидуальных особенностей больного, патологического процесса, вида и объема операции. Большая трубка затрудняет интубацию и делает ее травматичной, а маленькая трубка трудно фиксируется и может далеко проходить в бронх. При узкой трубке затрудняется поддержание адекватной ИВЛ, что приводит к гипоксии и гиперкапнии. Сопротивление каждого канала трубки может достигать 4 - 7 см вод. ст., что важно учитывать при выборе режима ИВЛ. К недостаткам метода раздельной интубации бронхов относится возможность попадания инфицированного материала в здоровые отделы оперируемого легкого, например при лобэктомии. Временное коллабирование легкого и тщательная аспирация бронхиального содержимого способствуют защите здоровых отделов.
Контроль за положением двухпросветных трубок осуществляют визуально (экскурсии грудной клетки), аускультативно (с попеременным выключением легкого) и при необходимости рентгенологически. Для соединения двухпросветных трубок с наркозным аппаратом применяют специальные коннекторы, позволяющие проводить раздельную вентиляцию легких, аспирировать секрет из бронха одного легкого, не прекращая вентиляции другого, создавать «управляемый» коллапс легкого.
Выбор общего анестетика для поддержания анестезии при операциях на легких осуществляется с учетом следующих требований: препарат должен быть малотоксичным, легко управляемым, невзрывоопасным, обеспечивать необходимую глубину наркоза при достаточном содержании кислорода в газонаркотической смеси и не влиять отрицательно на органы дыхания. Наиболее часто применяют закись азота в смеси с фторотаном или в сочетании с препаратами для НЛА, метоксифлуран, а в последние годы - этран. Для достижения миоплегии используют релаксанты как деполяризующего, так и недеполяризующего типа.
Для коррекции гиповолемии целесообразно использовать метод гемодилюций (для предотвращения «сладж-синдрома»). Важно избегать глубокого уровня общей анестезии (не более III2 стадии) для раннего пробуждения больного и восстановления кашлевого рефлекса.
Премедикация, введение и поддержание анестезии принципиально не отличаются от таковых при операциях на легких. Особые трудности возникают при выборе метода интубации для поддержания адекватного газообмена при операциях, предусматривающих резекцию главных бронхов и трахеи (пластические операции). Для проведения ИВЛ при реконструктивных операциях на трахее и бронхах разработаны различные способы ИВЛ по типу шунт-дыхание в зависимости от характера патологического процесса, операционного доступа, особенностей методики операции.
При резекции шейного отдела трахеи применяют двухэтапную интубацию - вначале трубку проводят через голосовую щель в подсвязочное пространство трахеи, а затем, после трахеотомии,- в нижний отдел и через нее осуществляют ИВЛ. При резекции грудного отдела трахеи после интубации подсвязочного пространства (в первый этап операции) осуществляют интубацию нижнего отрезка трахеи через операционную рану после ее вскрытия или пересечения при трансстернальном доступе. Интубационную трубку выбирают достаточной длины с таким расчетом, чтобы при необходимости ее можно было продвинуть ниже уровня резекции. При трансплевральном доступе применяют этот же способ или интубируют левый главный бронх через разрез в правом бронхе. При операциях на бифуркации трахеи рекомендуется интубировать один из пересеченных бронхов со стороны переднего средостения или правой плевральной полости [Петровский Б. В. и др., 1976]. В качестве методов обеспечения газообмена при операциях на трахее и ее бифуркации используют также искусственное кровообращение, гипербарическую оксигенацию, гипотермию, инжекционную вентиляцию. Для профилактики нарушений газообмена в связи с длительным выключением одного легкого прибегают к периодической вентиляции его через вторую трубку, введенную в пересеченный бронх. ИВЛ проводят в режиме гипервентиляции, параллельно корригируют сдвиги КЩС.
При операциях на легких, трахее и бронхах важно сохранять проходимость трахеобронхиального дерева (постоянная или периодическая аспирация содержимого через интубационную трубку, проверка герметичности швов), умеренно и постепенно повышать давление на вдохе до 20 - 30 мм вод. ст., тщательно расправлять оставшиеся отделы легочной ткани, создавать отрицательное давление в плевральной полости перед зашиванием грудной стенки.






