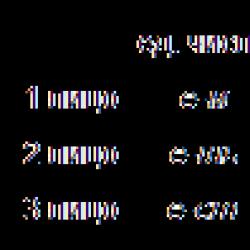Дистрофия у детей и взрослых, питание при дистрофии
– заболевание, вызванное хроническими расстройствами питания и сопровождающееся атрофией тканей. Дистрофия встречается у пациентов любого возраста, но особенно опасна для детей первых лет жизни. Заболевание в раннем возрасте может привести к нарушениям обменных процессов, снижению иммунитета, задержке физического и интеллектуального развития. Средние и тяжёлые формы дистрофии редко диагностируются в социально благополучных регионах. Диагноз «пренатальная (внутриутробная) дистрофия» ставится четверти недоношенным младенцам.
Дистрофия не обязательно характеризуется дефицитом массы тела к росту, как это свойственно всем пациентам-гипотрофикам. При другой разновидности дистрофии, паратрофии, наблюдается преобладание массы тела человека над его ростом и развитие ожирения. Равномерное отставание и роста, и массы тела от возрастных норм – ещё один вариант дистрофии гипостатурного типа. Наиболее распространён и опасен первый вид заболевания – гипотрофная дистрофия.
Причины
Первичная алиментарная дистрофия в пренатальном периоде вызывается нарушениями плацентарного кровообращения и внутриутробной гипоксией плода. К факторам риска во время беременности относят: возраст пациентки до 20 и после 40 лет, инфекционные заболевания в любом триместре, тяжёлые соматические заболевания, включая травмы, хронические и наследственные болезни, патологии плаценты, гестозы или токсикозы в любом триместре, неблагоприятная социальная среда, приводящая к нервным стрессам и нерациональному питанию, курение.
Первичная приобретённая дистрофия может стать следствием некачественного питания с белково-энергетическая дефицитом или результатом недостаточного питания в тяжелых социальных условиях. К первичной дистрофии могут также привести повторяющиеся инфекционные заболевания, вызванные кишечными и ротавирусными инфекциями, рецидивирующим отитом.
Вторичная дистрофия пре- и постнатального периода сопровождаёт врождённые и приобретённые: пороки развития, хромосомные заболевания, первичную или вторичную энзимопатию, выраженную в отсутствии или нарушении активности какого-либо фермента, первичную или вторичную мальабсорбцию, характеризующуюся нарушениями всасывания в тонком кишечнике, иммунодефицитные состояния.
Возникновение паратрофии обычно соотносят с избыточной калорийностью пищи и высоким содержанием в пищевом рационе углеводов и жиров. Развитие паратрофии провоцирует диатез лимфатико-гипопластического и экссудативно-катарального типов с увеличением лимфоидной ткани, а также с воспалением и покраснением эпителия и слизистых оболочек. Дистрофия гипостатурного характера связана с серьёзными поражениями нейроэндокринной системы.

Симптомы
Гипотрофия первой степени характеризуется дефицитом массы тела около 10-20% по сравнению с физиологической нормой. Состояние пациента – удовлетворительное, с незначительным снижением аппетита, тургора кожи и уменьшением подкожных жировых отложений. При второй степени гипотрофии с дефицитом массы тела до 30% у пациента снижен эмоциональный тонус и двигательная активность. Больной – апатичен, мышечный тонус и тургор тканей существенно снижен. У него значительно уменьшено количество жировой клетчатки в области живота и конечностей. О нарушениях терморегуляции свидетельствуют колебания температуры тела и холодные конечности. Дистрофия второй степени сопровождается нарушениями в работе сердечно-сосудистой системы с приглушённостью сердечных тонов, тахикардией, артериальной гипотензией.
Гипотрофию третьей степени с дефицитом массы тела более 30% ещё называют атрофией или алиментарным маразмом. На этой стадии развития заболевания общее состояние пациента серьёзно нарушено, больной склонен к сонливости, безучастности, раздражительности, анорексии. При гипотрофии третьей степени нет подкожной жировой клетчатки. Мышцы полностью атрофированы, но их тонус повышен из-за существующих неврологических нарушений и расстройств электролитного баланса. Гипотрофия сопровождается обезвоживанием, сниженной температурой тела, артериальной гипотензией, редким и слабым пульсом. Дискинетические проявления дистрофии проявляются в срыгивании, рвоте, учащённом жидком стуле, редком мочеиспускании.
Гипостатура является проявлением пренатальной дистрофии нейроэндокринного типа. Врождённая гипостатура диагностируется при рождении ребёнка по характерным клиническим признакам: функциональным расстройствам ЦНС и внутренних органов, признакам нарушения метаболизма, бледности и сухости кожных покровов, по снижению тургора тканей и низкой сопротивляемости ребёнка к инфекциям. Стойкие врождённые нарушения эндокринной и нервной регуляции процессов слабо поддаются лечению. При отсутствии выше перечисленных клинических симптомов и имеющимся одновременным отставанием физиологических показателей массы и роста от возрастных норм гипостатура может оказаться следствием конституциональной низкорослости.
Паратрофия у детей, как правило, провоцируется перекормом или несбалансированным питанием с избыточным содержанием углеводов и недостаточным количеством белка. К паратрофии более склонны малоподвижные дети на искусственном вскармливании с различными видами диатеза. Длительное перекармливание и систематичная гиподинамия нередко приводят к ожирению, как одному из проявлений дистрофии паратрофического типа. К клиническим симптомам паратрофии относят неустойчивый эмоциональный тонус, вялость, головные боли, одышку, быструю утомляемость. Аппетит нередко снижен и имеет избирательный, характер. На фоне избыточной подкожной жировой клетчатки наблюдается недостаточная эластичность кожных покровов и сниженный мышечный тонус. Возможны морфологические и функциональные трансформации внутренних органов на фоне снижения иммунитета.
Диагностика
Постановка диагноза «дистрофия» осуществляется на основе характерных клинических признаков, включая соотношение массы тела к росту, оценку тургора тканей, количество и размещение подкожной жировой клетчатки, анализ сопротивляемости организма к инфекционным заболеваниям. Степень гипотрофии определяется по результатам лабораторных исследований крови и мочи. Гипотрофия первой степени — лабораторные исследования крови и желудочной секреции указывают на диспротеинемию, выраженную в дисбалансе фракций белков крови и сниженную активность пищеварительных ферментов.
Гипотрофия второй степени — по данным лабораторных исследований у пациентов с дистрофией на этой стадии ярко выраженная гипохромная анемия со сниженным количеством гемоглобина в крови. Также диагностируется гипопротеинемия с низким содержанием общего белка в крови на фоне значительного снижения ферментной активности. Гипотрофия третьей степени — лабораторные исследования указывают на сгущение крови с замедленной скоростью оседания эритроцитов и наличие в моче значительных количеств мочевины, фосфатов, хлоридов, иногда ацетона и кетоновых тел.
Дифференционный диагноз «гипостатура» устанавливается методом исключения заболеваний, сопровождающихся отставанием физического развития, например, гипофизарного нанизма, при котором гипофиз человека не вырабатывает достаточного количества соматотропных гормонов, или других мутационных типов нанизма с достаточной секрецией соматропина, но нечувствительностью к нему организма. Другими вариантами генетически обусловленной низкорослости могут быть различные формы дистрофий, выраженные в аномальных пропорциях скелета. Изучение семейного анамнеза позволяет дифференцировать паратрофию и гипостатуру от семейной конституциональной низкорослости.
Лечение
Основополагающим аспектом рационального лечения дистрофии является диетотерапия. Первоначально выясняется переносимость пищи организмом, в случае необходимости назначаются ферменты: абомин, фестал, панзинорм, панкреатин. На следующем этапе проводится постепенная коррекция объёма и энергетической ценности употребляемой пищи с регулярным контролем характера стула и диуреза, набора или убавления массы тела. Для этих целей заводится специальный пищевой дневник с занесением количества и наименований продуктов. Питание дробное, малыми порциями до 10 приёмов пищи в сутки. Контроль осуществляется до достижения пациентом физиологических норм веса.
В качестве стимулирующей терапии применяются мультивитаминные комплексы и курсы общетонизирующих средств: препараты с женьшенем, маточным молоком, лимонником, овсом. Также проводится санирование очагов хронической инфекции, терапия сопутствующих заболеваний. Устранение гиподинамии и повышение эмоционального статуса достигается при помощи массажа, выполнения комплекса лечебных физических упражнений.
Профилактика
Пренатальная профилактика, направленная на предупреждение развития внутриутробной дистрофии, включает в себя: полноценный сон, режим работы и отдыха, сбалансированное питание, посильные физические упражнения, контроль веса женщины, регулярный мониторинг состояния здоровья женщины и плода. Постнатальная профилактика дистрофии у ребёнка наилучшим образом осуществляется при естественном вскармливании, постоянном контроле над ежемесячными прибавлениями роста-веса в течение первого года и ежегодном мониторинге дальнейшей динамики физического развития. Предупреждение дистрофии у взрослых пациентов возможно при условии достаточного питания, заместительной терапии энзимопатии и мальабсорбции, а также лечения основных иммунодефицитных состояний.
В современной неврологии существует огромное количество заболеваний, характер возникновений которых не поддаются рациональному объяснению со стороны специалистов. К таким болезням можно отнести группу таких недугов, как мышечная дистрофия. Всего разновидностей данной болезни девять, но обо всем по порядку…
Мышечная дистрофия - это хроническое наследственное заболевание в результате развития которого происходит поражение мышечной системы человека. Пораженные мышцы перестают нормально функционировать, истончаются в размерах, а в месте их расположения в организме постепенно нарастает жировая прослойка.
Разновидности мышечной дистрофии
В современной неврологии данный недуг классифицируется на девять различных болезней. Классификация заболевания связана с:
- локализацией мышечных нарушений;
- характеристиками болезни;
- агрессивностью развития;
- возрастом.
Так, мышечная дистрофия бывает:
- Дюшенна;
- миотоническая (болезнь Штейнерта);
- Беккера;
- Эрба Рота;
- юношеская форма дистрофии Эрба-Рота;
- плече - лопаточная лицевая форма (Ландузи-Дежерина);
- алкогольная миопатия;
- дистальная форма;
- миодистрофия Эмери -Дрейфуса.
Дистрофия Дюшенна
Наиболее известная форма прогрессирующая дистрофия Дюшенна (псевдогипертрофическая дистрофия, мерозин - негативная врожденная дистрофия). Данная разновидность недуга проявляется в детском возрасте начиная с двух до пяти лет. В первую очередь от данного недуга страдают мышцы нижних конечностей, которые несмотря на малоподвижный образ жизни у маленьких пациентов, постепенно увеличиваются в размерах. Данная особенность связана с нарастанием жировой ткани вместо мышц.

Слева здоровый ребенок, справа больной
Постепенно, по мере прогрессирования болезни она переходит в верхнюю часть и поражает мышцы верхних конечностей. Как правило, уже к двенадцатилетнему возрасту маленький пациент перестает полностью двигаться. Летальность у данного заболевания очень высока примерно 85–90% больных не доживают до 20-летнего возраста.
В группе риска находятся представители мужского пола, так как девочек данный недуг практически не затрагивает.
Болезнь Штейнерта
Врожденная дистрофия Штейнера не зря имеет название миотоническая, так как в результате прогрессирования болезни происходит слишком медленное расслабление мышц после их сокращения (такое явление называется миотонией).
Данное заболевание, в отличие от предыдущего распространено у взрослых, в возрасте от 20 до 40 лет. Имеют место быть и случаи прогрессирования болезни у детей, как правило, в младенческом возрасте, однако, это скорее исключение, чем правило.

На лицо признаки миотонии (приоткрытый рот и веки)
Гендерной зависимости болезнь не имеет и в равной степени от нее страдают как мужчины, так и женщины. Отмечается, что при недуге проявляется слабость мимических мышц лица, а также конечностей. Прогрессирование, в отличие от болезни Дюшенна происходит медленно.
Отличительная черта заболевания, возможность поражения не только мышц конечностей, но и внутренних мышц (сердечная мышца), что в свою очередь, представляет большую опасностью для жизни человека.
Болезнь Беккера
Данная форма болезни также долго прогрессирует, и пациент длительное время чувствует себя хорошо. Обострение недуга может произойти на фоне полученных травм или различных заболеваний нервной системы, которые своим течением ускорят развитие недуга.
В группе риска находятся люди низкого роста.
Болезнь Эрба-Рота и юношеская ее форма
Данное аутосомно - рецессивное заболевание развивается у пациентов после 20 лет, а юношеская форма у детей и подростков 11-13-летнего возраста. Прогрессирование болезни происходит по восходящему варианту, то есть сначала поражаются мышцы нижних конечностей, и постепенно происходит восхождение недуга к верхним конечностям.
Отличительной чертой недуга является наличие выступающих лопаток, которые по мере прогрессирования выступают более явно и очевидно.
Во время ходьбы отмечается переваливание пациента, выпячивание живота и задвигание грудной клетки.
Болезнь Ландузи-Дежерина
Плече-лопаточно-лицевая форма данного заболевания является наиболее безразборным видом, так как поражает людей в возрасте от пяти до 55 лет. Для данного недуга характерно очень длительное развитие, пациент может сохранять трудоспособность до 25 лет жизни с данной болезнью.
Отличительными симптомами является поражение лицевых мышц, в результате чего у больного могут возникнуть проблемы с четкостью произношения, в связи с неполным смыканием губ. Кроме того, отмечается неполное смыкание век.
По мере развития у больного атрофируются лицевые мышцы, мышцы плеч, конечности и туловища.
Данная форма не зависит от генетической мутации.
Алкогольная миопатия
Данный вид болезни также несвязан с генными мутациями и причина его возникновения одна - злоупотребление алкоголем. У больных могут отмечаться болевые синдромы в конечностях, связанные именно с поражением мышц.
Различают острую и хроническую алкогольную миопатию.
Дистальная форма
Дистальная форма мышечной дистрофии является доброкачественным вариантом прогрессирующей дистрофии. Как правило, данное заболевание трудно дифференцировать от невральной амиатрофии Мари-Шарко. Для разделения этих двух заболеваний требуется проведение электроэнцефалограмму головы, которая и дает понимание с какой болезнью предстоит иметь дело.
К основным симптомам недуга относят атрофию мышц конечностей с их последующим исхуданием. Возможны парезы стоп, кистей рук и т. п.
Миодистрофия Эмери -Дрейфуса
Данный тип болезни первоначально, вообще, не был выделен в качестве отдельного заболевания, так как по своей симптоматике был схож с дистрофией Дюшенна. Однако, в дальнейшем в результате длительного исследования было установлено, что болезнь Эмери -Дрейфуса обладает индивидуальной симптоматикой.
Болезнь относят в разряд редких. В группе риска находятся люди до 30 лет, как правило, юный возраст. Есть свидетельства о проявлении симптомов и после 30 лет, но они единичны.
Основное отличие данного вида болезни - это проблемы с мышцами сердца, которые в итоге могут стать причиной смерти. Кардиомиопатия при данном недуге не единственное отличие. Кроме проблем с сердцем, у пациентов наблюдают стандартные для дистрофии Дюшенна признаки, но в более щадящем режиме развития.
Причины
Негативная составляющая болезней нервной системы заключается в том, что они тяжело поддаются изучению. По этой причине не до конца известно о факторах, провоцирующих развитие той или иной формы мышечной дистрофии.
Основная причина, для формирования большинства подвидов данной болезни является генная мутация, в частности гена, который отвечает за синтез белка.
К примеру, болезнь Дюшенна имеет прямое отношение к мутации половой Х хромосомы. Основной переносчик нехорошего гена выступают девушки, которые несмотря на его наличие в собственной ДНК не страдают от данной болезни.
Что касается миотонической формы, то виновник ее возникновения ген, расположенный в 19 хромосоме.
Основные симптомы
Наличие большого количество различных подвидов у данного недуга указывает на различия в симптоматике, однако у болезни есть общие симптомы, которые в себя включают:

Диагностика мышечной дистрофии
Диагностические мероприятия при подобном недуге обширны, так как существует большое количество болезней, от которых необходимо дифференцировать болезнь.
На первоначальном этапе доктор обязательно изучит анамнез больного, уточнит о симптоматике, режиме дня и т. п. Эти данные требуются для составления плана проведения последующих диагностических мер, которые могут в себя включать:

Стоит отметить, что чем позже проявилась болезнь, тем лучше для больного, так как ранние симптомы в большинстве случаев заканчиваются смертью.
Лечение
Лечение мышечной дистрофии процесс сложный и затяжной, однако, в настоящее время не создано лекарство, которое полностью исцеляет больного. Все мероприятия направлены на облегчение жизни больного и восстановления некоторых утраченных способностей.
Для затормаживания развития болезни назначают следующие препараты:
- кортикостероиды;
- витамины В1;
- аденозинтрифосфат (АТФ).
Кроме того, для замедления процесса развития используют фетальные стволовые клетки, которые замедляют процесс дистрофии.
Помимо того, в качестве профилактических мероприятий назначают:
- массаж;
- физиотерапию;
- дыхательную гимнастику.
Помимо стандартных вариантов лечения, важно постоянно руководствоваться тремя главными составляющими в процессе жизнедеятельности:
- Адекватная физическая активность.
- Своевременная психологическая поддержка.
- Соблюдение диеты.
Физическая активность
Отсутствие желания у человека бороться с недугом оказывает негативное воздействие на организм. Судите сами, пассивность, нежелание двигаться угнетает и без того пораженную мышечную систему. Мышцам необходимо давать нагрузку, так как без нагрузки дистрофичные процессы начинают происходить быстрее, тем самым прогрессируя в более быстром темпе.
Умеренная физическая активность, использование поддерживающих приспособлений будут отличным подспорьем в борьбе с недугом.
При наличии болей в мышцах отлично подойдет плавание, йога, упражнения на растяжку.
Психологическая поддержка
Психологическая поддержка окружения важна для больного человека. А если недуг такой серьезный, как этот тем более. Для кого-то будет достаточно обычной поддержки со стороны друзей и родных, а кому-то может потребоваться квалифицированная психологическая помощь.
Важно дать понять такому человеку, что он не остался один на один со своей проблемой. Он должен понимать, что ему есть к кому обратиться, есть люди, которые сопереживают и поддерживают его.
Диета
Что касается режима питания и соблюдения диеты, существует расхожее мнение, что соблюдение противовоспалительной диеты может замедлить прогрессирование недуга. Данная диета снижает воспаление, уровень глюкозы, выводит токсины из организма и питает его полезными веществами.
Суть такой диеты в следующем:
- Отказ от продуктов, содержащих «плохие» жиры и замена их на «хорошие», введение в рацион ненасыщенных жиров, которые содержатся в оливковом, льняном, кунжутном масле, авокадо.
- Применение в пищу мяса и рыбы, при производстве которых не были использованы антибиотики или гормоны.
- Полное удаление из рациона рафинированного сахара и глютена.
- Употребление в пищу следующих продуктов - китайская капуста, брокколи, сельдерей, ананас, лосось, свекла, кукумария, имбирь, куркума и других продуктов, обладающих противовоспалительными свойствами.
- Молочные продукты допустимы только на основе овечьего и козьего молока.
- Допустимо употребление травяных чаев, лимонада, кваса, морсов и натуральных соков.
Профилактика
Так как мышечную дистрофию довольно тяжело предсказать и обнаружить на раннем этапе, профилактические мероприятия сводятся к двум простым рекомендациям:
Обязательное обследование женщины на этапе планирования беременности на предмет наличия мутаций в генах
В случае если до беременности, по каким-либо причинам не было сделано генетического обследования, уже в период беременности проводится тест на определение у плода мутаций в Х хромосоме.
Прогноз и осложнения
В зависимости от вида болезни прогноз может быть разным, и тем не менее можно выделить несколько возможных осложнений, возникающих при данном недуге.
- нарушения сердечной деятельности
- искривление позвоночника
- снижение интеллектуальных способностей больного
- снижение двигательной активности
- нарушения дыхательной системы
- летальный итог
Итак, мышечная дистрофия довольно опасное и неизлечимое заболевание, поэтому будущим родителям необходимо с глубокой ответственностью относиться к планированию беременности. Берегите себя и своих будущих детей!
 Дистрофия
– это патологический процесс, ведущий к структурным изменениям в органах и тканях. В основе дистрофии чаще всего лежат метаболические нарушения, но также дистрофия может быть наследственным заболеванием (например, пигментная дистрофия сетчатки
). При этом процессе повреждаются клетки и межклеточное вещество, что приводит к потере их функции. Таким образом, из строя выходит целый орган. Например, при дистрофии роговицы отмечается повреждение ее слоев, в результате чего она становится мутной и перестает выполнять основную свою функцию.
Дистрофия
– это патологический процесс, ведущий к структурным изменениям в органах и тканях. В основе дистрофии чаще всего лежат метаболические нарушения, но также дистрофия может быть наследственным заболеванием (например, пигментная дистрофия сетчатки
). При этом процессе повреждаются клетки и межклеточное вещество, что приводит к потере их функции. Таким образом, из строя выходит целый орган. Например, при дистрофии роговицы отмечается повреждение ее слоев, в результате чего она становится мутной и перестает выполнять основную свою функцию.Существует большое разнообразие дистрофий, классифицирующихся по системам, органам, причинам и так далее.
Жировая дистрофия печени
 Жировая дистрофия печени или жировой гепатоз – это синдром, проявляющийся различными повреждениями на клеточном уровне. Прежде чем приступить к описанию жировой дистрофии необходимо знать, что в зависимости от причины разделяют алкогольную и неалкогольную жировую дистрофию. Оба синдрома характеризуются одинаковыми морфологическими изменениями, а именно - жировой дистрофией и воспалительной реакцией. Разницей является то, что алкогольная дистрофия печени развивается у людей, злоупотребляющих алкоголем. При неалкогольной дистрофии наблюдаются те же изменения, но для пациентов с этой патологией не характерно систематическое употребление спиртных напитков.
Жировая дистрофия печени или жировой гепатоз – это синдром, проявляющийся различными повреждениями на клеточном уровне. Прежде чем приступить к описанию жировой дистрофии необходимо знать, что в зависимости от причины разделяют алкогольную и неалкогольную жировую дистрофию. Оба синдрома характеризуются одинаковыми морфологическими изменениями, а именно - жировой дистрофией и воспалительной реакцией. Разницей является то, что алкогольная дистрофия печени развивается у людей, злоупотребляющих алкоголем. При неалкогольной дистрофии наблюдаются те же изменения, но для пациентов с этой патологией не характерно систематическое употребление спиртных напитков.Характеристика жировой дистрофии на клеточном уровне
При данном заболевании в клетках печени выявляются патологические включения жира. Капельки жира, находящиеся в гепатоцитах, деформируют и нарушают функцию клеток. В результате этого в них отмечаются нарушения клеточного метаболизма , ведущие к структурным изменениям. Клетки печени (гепатоциты
) и межклеточное вещество погибают, что приводит к изменению функции самого органа. Морфологический диагноз жировой дистрофии ставится тогда, когда содержание жира в печени превышает 10 процентов от массы органа.
Печень – это жизненно важный орган, осуществляющий множество функций. Так, она несет ответственность за детоксикацию организма, синтез гормонов , обезвреживание различных чужеродных веществ. Именно поэтому малейшее нарушение структуры печени приводит к разнообразным и многочисленным симптомам. Основной причиной развития жировой дистрофии считают повышенное содержание в печени свободных жирных кислот .
Неалкогольная жировая дистрофия печени
Синонимами жировой дистрофии печени являются термины – жировой гепатоз, жировой стеатоз, первичная жировая дистрофия. Неалкогольная жировая дистрофия, как правило, протекает доброкачественно и бессимптомно. Крайне редко развивается цирроз печени , гепатит или печеночная недостаточность . Выявлено, что менее 10 процентов пациентов, страдающих хроническим гепатитом, ранее были диагностированы с жировой дистрофией. Впервые, как самостоятельное заболевание, данный синдром был выделен в 1980 году. На сегодняшний день частота выявления этой патологии варьирует от 7 до 10 процентов. Для сравнения, алкогольная жировая дистрофия диагностируется в 15 раз чаще.Причинами первичной жировой дистрофии являются:
- сахарный диабет 2 типа;
- гиперлипидемия (повышенное содержание липидов в плазме крови ).
Медикаментами, вызывающими жировую дистрофию, являются:
- амиодарон;
- синтетические эстрогены ;
- нестероидные противовоспалительные средства .
Механизм формирования жировой дистрофии
Почвой для формирования жировой дистрофии печени является повышенная концентрация свободных жирных кислот в крови. В норме жирные кислоты накапливаются в жировой ткани, в форме триглицеридов. По мере необходимости они поступают в печень или мышцы, где и происходит их утилизация. Необходимость возникает по время сильного стресса , физических нагрузок или голодания . При этих состояниях происходит расщепление жиров на свободные жирные кислоты и глицерин. После этого происходит транспортировка жирных кислот в печень и их окисление. Когда в печень поступает слишком много кислот, скорость их окисления в митохондриях печени снижается. Таким образом, происходит накопление жиров с их последующим отложением в клетках печени. Когда в гепатоците (печеночной клетке
) накапливается слишком много капель жира, клетка начинает деформироваться и терять свою функцию. Данный процесс и называется жировой дистрофией.
Далее происходит процесс, называемый стеатогепатитом. Для него характерно воспалительно-некротические изменения в паренхиме печени. Причиной этого процесса является перекисное окисление липидов. В результате перекисного окисления формируются свободные радикалы, которые и оказывают повреждающее действие на клетки печени. В зависимости от объема капель жира, а также от их количества, выделяют несколько степеней жировой дистрофии.
Степенями жировой дистрофии являются:
- нулевая степень – в отдельных группах печеночных клеток присутствуют мелкие капельки жира;
- первая степень – в гепатоцитах присутствуют умеренно крупные капли жира;
- вторая степень – отмечается феномен внутриклеточного ожирения, для которого характерно диффузное (распространенное ) крупнокапельное отложение жира;
- третья степень – капли жира отлагаются не только в клетке, но и вне ее (внутриклеточное и внеклеточное отложение жира ); также характерно формирование жировых кист.
Симптомы жировой дистрофии печени
Неалкогольная жировая дистрофия отмечается преимущественно у женщин. По последним данным женщин с этим заболеванием в два раза больше, чем мужчин. Чаще всего данная патология регистрируется в среднем возрасте (30 – 40 лет ). Основной симптом жирового гепатоза – это умеренно увеличенная печень. Далее клиническая картина дополняется симптомами печеночной дисфункции.Симптомами жировой дистрофии являются:
- боль в правом подреберье;
- астеновегетативные расстройства;
- повышение массы тела.
Боль в правом боку – является одним из самых частых симптомов, отмечается он у 60 процентов больных. Причиной болевого синдрома является растяжение фиброзной капсулы, которая покрывает печень. В самой печени нет нервных окончаний, поэтому любые ее повреждения не сопровождаются болевой симптоматикой. Однако сверху печень покрыта оболочкой, которая обильно снабжена нервными окончаниями. Когда печень увеличена (как при жировой дистрофии ), то капсула, ее покрывающая, растягивается, что провоцирует раздражение нервных окончаний. Поэтому, чем больше увеличена печень, тем выраженнее болевой синдром. При жировой дистрофии печени боль постоянная, тупая и ноющего характера.
Диспепсия
Диспепсические явления при жировой дистрофии печени отмечаются более чем у 45 процентов больных. Связаны они с застоем желчи и дефицитом желчных кислот в процессе пищеварения. Так, желчные кислоты расщепляют жиры на мелкие частицы, тем самым, обеспечивая их усваивание. При дефиците желчи этого не происходит, и поэтому у части больных возникает непереносимость жирной пищи. Также диспепсия при жировом гепатозе включает чувство тяжести в животе, тошноту и неустойчивый стул.
Астеновегетативные расстройства
Данная симптоматика встречается у одной трети больных с жировой дистрофией печени. Проявляется она такими симптомами как утомляемость , слабость , головная боль . Причиной этих симптомов, может быть недостаток витаминов или гиповитаминоз . Так, в печени синтезируются некоторые витамины. Однако при повреждении ее функции синтез витаминов снижается и развивается гиповитаминоз.
Повышение массы тела
Рост индекса массы тела отмечается более чем у 45 процентов больных. Объясняется данная симптоматика нарушением метаболизма.
Алкогольная дистрофия печени
Алкогольная дистрофия печени – это поражение печени, которое развивается вследствие систематического употребления алкоголя. Этанол оказывает токсическое действие на клетки печени, что приводит к развитию алкогольного гепатита. Известно, что основным местом метаболизма алкоголя является печень. Незначительная часть метаболизируется в легких и почках . Это и объясняет столь частое повреждение печени при хронической алкогольной интоксикации .Метаболизм алкоголя (этанола
)
Под действием печеночных ферментов происходит распад этанола на ацетальдегид. При этом высвобождается определенное количество калорий (на 500 миллилитров этанола приходится 1400 калорий
). Но при окислении этанола высвобождающиеся калории не имеют питательной ценности. Это приводит к тому, что имеющиеся резервы организма, а именно белки и жиры, начинают распадаться. Чем больше этанола окисляется, тем больше жиров разрушается. Таким образом, жир становится основным источником «топлива» для организма, что и запускает процесс алкогольной жировой дистрофии.
Помимо вышеперечисленного процесса на печень оказывает влияние прямое токсическое действие алкоголя.
Стадии алкогольной дистрофии печени
Алкогольное повреждение печени нередко заканчивается гепатитом или циррозом. То, насколько быстро прогрессирует болезнь, зависит от многих факторов, а именно от пола, возраста, сопутствующих заболеваний. При этом важно отметить, что до определенной стадии все изменения в печени обратимы. Это значит, что при своевременном отказе от систематического употребления алкоголя происходит восстановление прежней, нормальной структуры печени. Объясняется этот феномен высокой регенеративной (восстановительной ) способностью печени.Стадиями алкогольной дистрофии печени являются:
- первая стадия – собственно жировая дистрофия печени;
- вторая стадия – алкогольный гепатит печени;
- третья стадия – алкогольный цирроз печени.
Первая стадия алкогольного повреждения печени встречаются у 60 процентов лиц, злоупотребляющих алкоголем. Для этой стадии характерны те же изменения, что встречаются и при жировой дистрофии печени. Отложение жира в гепатоцитах происходит в форме больших крупных капель. Основным клиническим признаком является увеличение печени, то есть гепатомегалия . Печень на этой стадии увеличена умеренно - на 3 – 4 сантиметра. Поэтому основной жалобой со стороны пациента является боль. Увеличенная печень растягивает покрывающую ее капсулу и раздражает нервные окончания, что и обуславливает боль. Также в клинической картине на данном этапе присутствуют такие симптомы как тошнота, горечь во рту , неустойчивый стул.
При врачебном осмотре пальпируется (прощупывается ) умерено увеличенная печень с гладкими округлыми краями. Данная характеристика печени очень важна при дифференциальном диагнозе. Первая стадия алкогольной дистрофии является полностью обратимой.
Вторая стадия алкогольной дистрофии печени
Продолжающееся злоупотребление спиртными напитками приводит к дальнейшему повреждению гепатоцитов. Перекисное окисление липидов приводит к повреждению мембран печеночных клеток и развитию воспалительной реакции. Типичным морфологическим признаком на этой стадии является наличие в гепатоцитах алкогольного гиалина. На второй стадии печень увеличивается на 10 – 15 сантиметров.
Алкогольный гепатит на второй стадии может быть как острым, так и хроническим. Острый алкогольный гепатит развивается внезапно, после длительного запоя. Хронический алкогольный гепатит развивается постепенно на фоне уже имеющихся повреждений печени.
Клиническая картина включает тупую боль в правом подреберье, рвоту , диарею , резкое похудение . Нередко развивается желтуха , для которой характерно желтушное окрашивание кожи и слизистых, а также кожный зуд . Все печеночные ферменты резко повышены, количество лейкоцитов поднимается, скорость оседания эритроцитов достигает 50 миллиметров в час. Как правило, эта стадия переходит в цирроз.
Третья стадия алкогольной дистрофии печени
Третья стадия или стадия цирроза диагностируется у 10 – 15 процентов людей, злоупотребляющих алкоголем. Основная морфологическая характеристика этой стадии – это формирование склеротических узлов и перестройка архитектоники печени. Разрушенные гепатоциты постепенно замещаются соединительной тканью, что приводит к деформированию структуры печени. Печень на этой стадии начинает уменьшаться в размерах, что является неблагоприятным признаком. В клинической картине появляются такие симптомы как асцит (в народе – водянка
), гинекомастия (увеличение молочных желез у мужчин
), желтуха.
Лечение жировой дистрофии печени
Лечение жировой дистрофии печени основано на комплексном применении витаминов, гепатопротекторов и других медикаментов. На первых стадиях возможен регресс заболевания и восстановление функции печени. На поздних стадиях жировой дистрофии проводится симптоматическое лечение. Целью лечения является замедление дистрофии и предупреждение развитие цирроза.К группам медикаментов, которые используются в лечении жировой дистрофии, относятся:
- витамины;
- гепатопротекторы;
- кортикостероиды.
Проводится всем пациентам вне зависимости от причины заболевания, так как у большинства отмечается дефицит витаминов. Особенно важна витаминотерапия при алкогольной жировой дистрофии. Витамины целесообразно назначать не в виде таблеток, а методом парентерального введения (внутримышечно или посредством капельницы ). Назначаются витамины В12, В1, B6, РР или комбинированных препараты, такие как мильгамма , демотон. Мильгамма назначается внутримышечно по одной ампуле в день курсом 10 дней, демотон - по одной ампуле через день.
Гепатопротекторы
Гепатопротекторы – это препараты, которые оказывают защитное воздействие на печень. Это очень большая группа препаратов, отличающихся по происхождению и механизму действия. С профилактической целью широко используется силимарин. Механизм его действия обусловлен подавлением синтеза коллагена клетками печени. Назначается в дозе 70 – 100 миллиграмм в сутки на протяжении 3 месяцев. Вместо силимарина может использоваться адеметионин. Доза адеметионина составляет от 800 до 1600 миллиграмм в сутки. В последнее время хорошо зарекомендовали себя эссенциальные фосфолипиды. Исследования показали, что наиболее эффективны они при алкогольной дистрофии печени. Аналогом фосфолипидов является препарат эссливер форте. Кроме эссенциальных фосфолипидов он содержит тиамин , рибофлавин, пиридоксин гидрохлорид, цианокобаламин и токоферола ацетат. Таким образом, эссливер форте не только препятствует синтезу коллагена, но и восполняет дефицит витаминов, который отмечается у алкоголиков. Препарат назначается по 2 капсулы 3 раза в сутки на протяжении полугода.
Кортикостероиды
Назначаются в исключительных случаях, например, при алкогольном гепатите либо у пациентов с печеночной энцефалопатией . Последние исследования показали, что частота летальных исходов у больных с алкогольным гепатитом снижается при применении 40 мг преднизолона в сутки в течение 4 недель. Реже рекомендуется пульс-терапия, которая основывается на применении высоких доз стероидов - от 300 миллиграмм в сутки на протяжении 2 – 3 дней.
Мышечные дистрофии
 Мышечные дистрофии – это группа наследственных заболеваний, в основе которых лежит дистрофия скелетных мышц. Клинически мышечные дистрофии проявляются мышечной слабостью, которая ограничивает двигательную способность пациента. Дебютируют мышечные дистрофии, как правило, еще в младенческом возрасте.
Мышечные дистрофии – это группа наследственных заболеваний, в основе которых лежит дистрофия скелетных мышц. Клинически мышечные дистрофии проявляются мышечной слабостью, которая ограничивает двигательную способность пациента. Дебютируют мышечные дистрофии, как правило, еще в младенческом возрасте.Механизм развития дистрофий заключается в нарушении функции произвольной мускулатуры. Так, в организме человека различают три вида мускулатуры - гладкая и скелетная мускулатура, а также миокард (сердечная мышца
). Из гладкой мышечной ткани состоят внутренние органы (желудок , кишечник
). Сокращение этого вида тканей происходит непроизвольно, человек не может ею управлять. Скелетная мускулатура – это та мышечная ткань, которая обеспечивает человеку движения. При мышечной дистрофии происходит поражение именно скелетной мускулатуры, то есть той, которая обеспечивает человеку движения.
К видам мышечных дистрофий относятся:
- дистрофия Дюшенна;
- мышечная дистрофия Беккера;
- миотоническая дистрофия.
Мышечная дистрофия Дюшенна
Это одна из самых часто встречающихся форм мышечных дистрофий. Причиной дистрофии Дюшенна является генетический дефект на хромосоме Х. Данный дефект обуславливает дефицит белка дистрофина, который в норме защищает мышцы от повреждений. При его недостатке мышцы быстро разрушаются и перестают нормально функционировать. Женщины с данным дефектом болезнь не проявляют, но могут передавать дефектный ген детям. Если ребенок мужского пола получил данный дефектный ген, у него развивается болезнь. Дебют заболевания приходит на возраст от 2 до 5 лет.Изначально дистрофия проявляется в мышцах нижних конечностей и мышцах таза. Далее «болезнь поднимается выше» и затрагивает верхние группы мышц. Морфологическим признаком болезни Дюшенна является дегенерация (разрушение ) мышечных волокон. На их месте начинает разрастаться жировая и соединительная ткань. Характерный признак данной патологии – это увеличение икроножных мышц. Это происходит за счет отложения в них жира, вследствие чего мышцы выглядят увеличенными. Данный феномен носит название псевдогипертрофии икроножных мышц и характерен он, преимущественно, для дистрофии Дюшенна.
К признакам дистрофии Дюшенна относятся:
- неуклюжая походка;
- частые падения;
- трудности при беге, прыжках;
- постоянная слабость;
- мышечные контрактуры (состояние, когда вследствие непроизвольного напряжения мышц ограничены функции работы сустава ).
На этой стадии симптомы болезни еще не появляются. Однако часто отмечается задержка
психоречевого и моторного развития у детей. Диагноз можно поставить только в том случае, если имеется отягощенный семейный анамнез (то есть, если в семье имелись случаи заболевания дистрофией Дюшенна ).
Ранняя стадия дистрофии Дюшенна
Основным симптомом ранней стадии является нарастающая мышечная слабость. При тщательном осмотре можно выявить некоторые положительные симптомы болезни. Например, при подъеме с пола ребенок опирается руками о колени. Данный диагностический симптом называется положительной пробой Говерса. Также может наблюдаться «утиная походка» - при этом ребенок опирается на передние отделы стоп.
Поздняя стадия дистрофии Дюшенна
Самостоятельная ходьба на этой стадии наблюдается редко. Ребенок не в состоянии передвигаться, подниматься с пола. Мышечная слабость затрагивает и верхние конечности. Отмечается дистрофия дыхательной мускулатуры и поражение сердца .
Диагностика дистрофии Дюшенна
Основывается на анамнестических данных, врачебном осмотре и специфических лабораторных тестах. При осмотре отмечается мышечная слабость и увеличение (псевдогипертрофия
) икроножных мышц. Родители ребенка отмечают, что он гораздо позже начал ползать, ходить. Также они могут отмечать позднее речевое развитие.
В обязательном порядке проводится генетический анализ, биопсия мышц и лабораторные анализы. В анализе крови выявляется повышенное содержание креатинфосфокиназы и печеночных ферментов. Биопсия мышц выявляет дефицит белка дистрофина в мышечных клетках.
Прогноз при дистрофии Дюшенна неблагоприятный, так как заболевание очень быстро прогрессирует. Больные погибают в возрасте 20 лет от дыхательной недостаточности или сердечной недостаточности .
Дистрофия Беккера
Дистрофия Беккера – это также генетически обусловленное заболевание, в основе которого лежат дегенеративные изменения в мышечных волокнах. Причиной является дефект в гене, кодирующем белок дистрофин.Дебют заболевания приходится на возраст 10 – 15 лет. Первый симптом – это мышечная слабость при интенсивных физических нагрузках. Далее слабость отмечается при умеренной нагрузке, например, при подъеме по лестнице. Способность к самостоятельному передвижению при дистрофии Беккера сохраняется до 40 лет.
Симптомами дистрофии Беккера являются:
- слабость в мышцах – 100 процентов;
- атрофия мышц таза – 90 процентов;
- псевдогипертрофия икроножных мышц – 80 процентов;
- снижение сухожильных рефлексов – 70 процентов.
Миотоническая дистрофия
Миотоническая дистрофия или болезнь Штейнерта встречается относительно редко. Ее развитие обусловлено генетическим дефектом в 19-й хромосоме. Она одинаково поражает как мужчин, так и женщин. Начало заболевания часто приходится на возраст 30 – 40 лет. Первые проявления болезни – это слабость мимических мышц, замедленное расслабление после сокращения мышц конечности. Особенностью данной формы является то, что кроме скелетной мускулатуры повреждается гладкая мышечная ткань внутренних органов.Лечение мышечных дистрофий
На сегодняшний день не существует специфических методов лечения мышечных дистрофий. Лечение направлено на борьбу с осложнениями - частые пневмонии , искривление позвоночника , сердечная недостаточность. Комплексное лечение включает физиотерапию , активные и пассивные упражнения, редко кортикостероиды. Иногда рекомендуется хирургическое лечение. Оно проводится с целью коррекции контрактур или сколиоза . Широко используются механические средства - подтяжки, инвалидные коляски, трости.При дистрофии Дюшенна назначаются кортикостероиды, такие как преднизолон и дефлазакорт. Данные препараты способны замедлить прогрессирование мышечной слабости и отсрочить утрату способности к самостоятельному передвижению на 2 – 3 года.
Дистрофия миокарда
 Дистрофия миокарда – это дегенеративное поражение мышц сердца, как правило, связанное с нарушением в них обмена веществ. Чаще всего дистрофия сердца или миокардиодистрофия
– это приобретенное заболевание. Миокардиодистрофии могут быть вызваны самыми различными причинами - недостаточным питанием , приемом некоторых лекарств, системными заболеваниями.
Дистрофия миокарда – это дегенеративное поражение мышц сердца, как правило, связанное с нарушением в них обмена веществ. Чаще всего дистрофия сердца или миокардиодистрофия
– это приобретенное заболевание. Миокардиодистрофии могут быть вызваны самыми различными причинами - недостаточным питанием , приемом некоторых лекарств, системными заболеваниями.Причинами дистрофии миокарда являются:
- недостаточное питание;
- токсическое воздействие алкоголя;
- системные заболевания.
Дистрофия сердца при диетах и несбалансированном питании
Поражение миокарда может быть спровоцировано как избыточным, так и недостаточным питанием. Чаще всего сердце поражается при безбелковой диете , голодании, недостаточном поступлении витаминов группы В, селена.К погрешностям в питании, которые сопровождаются дистрофией сердца, относятся:
- голодание;
- белковая недостаточность (квашиоркор );
- недостаток витаминов группы В;
- дефицит селена.
Как правило, отказ от пищи наблюдается при анорексии или при других психических расстройствах . Голодание приводит к дегенеративным изменениям миокарда. При длительном голодании снижается основной обмен и замедляется работа сердца. К морфологическим изменениям в миокарде относят жировую дистрофию на фоне атрофии. Клинически дистрофия миокарда в данном случае проявляется снижением частоты сердечных сокращений (брадикардией ), снижением артериального давления , отеками. Длительный недостаток витаминов и минералов приводит к электролитным расстройствам, а именно - дефициту калия и других электролитов. На электрокардиограмме (ЭКГ ) отмечается снижение вольтажа комплекса QRS, отклонение электрической оси сердца вправо. При дальнейшем голодании дистрофия миокарда может прогрессировать вплоть до сердечной недостаточности.
Дистрофия миокарда при квашиоркоре
Квашиоркор – это заболевание, которое встречается, преимущественно, в развивающихся странах, и связанно оно с недостаточным потреблением белка. Поскольку белки – это основные пластические вещества организма (они входят в состав клеток, ферментов
), то при их дефиците возникает полиорганная недостаточность. Клиническая картина квашиоркора включает задержку роста, гипотрофию , дистрофию мышц, в том числе и мышц сердца. Максимально симптомы выражены в возрасте от 5 до 6 лет. Очень рано появляются отеки, увеличивается печень и уменьшается сердце. На электрокардиограмме отмечаются те же изменения, что и при остром голодании - снижение вольтажа и изменение зубца Т. При квашиоркоре также страдает нервная система - дети становятся вялыми, апатичными.
Дистрофия миокарда при дефиците витаминов группы В
Витамины группы В являются составной частью многих ферментов, участвуют в окислительно-восстановительных реакциях. При их недостатке в первую очередь нарушается обмен углеводов. В результате этого в тканях (в том числе и в сердечной мышце
) накапливается пировиноградная и молочная кислота, а также уменьшается образование энергии. Таким образом, развивается тканевой ацидоз , который обусловливает недостаточность кровообращения. При гиповитаминозе В наблюдается высокий сердечный выброс и низкое периферическое сосудистое сопротивление. Клиническая картина характеризуется такими симптомами как сердцебиение , утомляемость, а иногда и нарушения сердечного ритма (аритмии
). Морфологические признаки дистрофии миокарда при гиповитаминозе включают интерстициальный отек и дегенерацию мышечных волокон. Диагностика заключается в определении концентрации витамина B.
Дефицит селена
Селен – это микроэлемент, преимущественно содержащийся в печени, почках, селезенке. В организме человека концентрация селена варьирует от 10 до 15 миллиграмм. Он входит в состав белков мышечной ткани, в том числе и сердца. При дефиците селена снижается активность определенных ферментов, что провоцирует накопление свободных радикалов и повреждение кардиомиоцитов (клеток сердца
). Недостаточное поступление в организм селена обусловливает развитие застойной кардиомиопатии , которая может протекать остро или хронически. При острой форме развивается кардиогенный шок, отек легких и тяжелые аритмии . Хроническая форма проявляется брадикардией, снижением сердечного выброса и развитием сердечной недостаточности.
Алкогольная дистрофия миокарда (миокардиодистрофия )
Токсическое воздействие на сердечную мышцу оказывает алкоголь, тяжелые металлы и некоторые лекарства.Алкогольная дистрофия миокарда
Систематическое употребление алкогольных напитков является одним из факторов риска миокардиодистрофии. Более чем в 45 процентов случаев алкоголизм становится причиной дилатационной кардиомиопатии. Последние исследования показали, что систематическое злоупотребление алкоголем на протяжении 5 лет приводит к развитию дистрофии миокарда у каждой пятой женщины и аналогичного заболевания у каждого четвертого мужчины.
Дистрофия миокарда объясняется как прямым токсичным действием этанола на сердечную мышцу, так и опосредованным действием промежуточных продуктов обмена. Так, в организме алкоголь метаболизируется до ацетальдегида, который обладает сосудорасширяющими свойствами, а также стимулирует секрецию катехоламинов . Последние участвуют в реакциях клеточного метаболизма, включая транспорт кальция, синтез белков и тканевое дыхание. Продукты обмена алкоголя накапливаются в митохондриях сердечной мышцы, нарушая функции клеток и изменяя метаболизм всего сердца. В миокардиоцитах накапливаются жиры, и развивается феномен жировой дистрофии. Также у алкоголиков отмечаются множественные гиповитаминозы. На сердце большое влияние оказывает дефицит витамина В.
Алкогольная дистрофия сердца чаше всего развивается после 10 лет систематического употребления алкоголя, как правило, после 35 – 40 лет. Проявляется она одышкой (сначала при физической нагрузке, а потом и в покое ), усталостью, слабостью, аритмиями. При алкогольной дистрофии сердца высок риск внезапной сердечной смерти.
Токсические дистрофии также развиваются при употреблении кокаина, героина, при лечении противоопухолевыми средствами.
Сердечная дистрофия при системных заболеваниях
Системные заболевания – это аутоиммунные заболевания соединительной ткани. Поскольку соединительная ткань входит в состав практически всех органов и тканей, то при этих заболеваниях наблюдается системное (полиорганное ) поражение внутренних органов. Дистрофия миокарда наблюдается при системной красной волчанке , склеродермии .У больных с системной красной волчанкой нарушения сердечной деятельности отмечаются в 80 процентах случаев (поражение сердца носит название волчаночного миокардита ). При этом в патологический процесс вовлекаются все структуры сердца - миокард, перикард, эндокард и сосуды сердца. Но больше воспаление затрагивает сердечную мышцу (миокард ) с развитием диффузного или очагового миокардита. У пациентов с волчаночным миокардитом на электрокардиограмме отмечается тахикардия , изменения сегмента ST-T, нарушениями сердечного ритма (аритмии и блокады ). Негативное действие на сердечную мышцу оказывают также глюкокортикоиды , которые используются в лечении самой системной красной волчанки. Длительное применение высоких доз глюкокортикоидов приводит к стероидной дистрофии. Пациенты жалуются на частые сердцебиения, боли в области сердца , одышку.
При системной склеродермии поражение сердца появляется уже спустя 2 – 3 года от начала заболевания. Морфологическими признаками дистрофии миокарда являются диффузный фиброз и некроз сердечной мышцы. Это значит, что сами миокардиоциты отмирают, а на их месте развивается соединительная ткань. Постепенно соединительная ткань замещает ткань миокарда. Однако эта ткань не может также эффективно сокращаться как сердечная, что и провоцирует развитие сердечной недостаточности. Нередко сердечная симптоматика при данном заболевании предшествует всем остальным симптомам. Пациенты предъявляют жалобы на боли в сердце, которые протекают по типу стенокардических. Они локализуются за грудиной, носят давящий или сжимающий характер, а также отдают в левую руку или лопатку.
Дистрофии глаза (сетчатки и роговицы )
 Дистрофии глаза – это группа заболеваний, характеризующиеся дегенеративными изменениями в различных структурах глаза. Так, при дистрофии сетчатки изменения затрагивают различные слои сетчатки, а при дистрофии роговицы наблюдаются изменения в слоях роговицы.
Дистрофии глаза – это группа заболеваний, характеризующиеся дегенеративными изменениями в различных структурах глаза. Так, при дистрофии сетчатки изменения затрагивают различные слои сетчатки, а при дистрофии роговицы наблюдаются изменения в слоях роговицы.Сетчатка – это внутренняя оболочка глазного яблока, в строении которой различают несколько слоев. В самой сетчатке выделяют центральный (он же макула ) и периферический отделы. Дистрофия сетчатки – это деструктивный (разрушающий ) процесс слоев сетчатки, чаще всего, вследствие нарушенного их питания. Дистрофические изменения могут быть врожденными (семейно-наследственными ) или приобретенными. У лиц пожилого возраста выявляются старческие дистрофии сетчатки, в развитии которых большое значение играет атеросклероз .
Видами дистрофии сетчатки являются:
- пигментная дистрофия сетчатки;
- дистрофия макулы;
- кольцевидная дистрофия сетчатки.
Пигментная дистрофия сетчатки
Эта патология, которая одновременно затрагивает оба глаза и сопровождается разрушением пигментного слоя сетчатки. Пигментный эпителий – это десятый слой сетчатки, который содержит в себе светочувствительные элементы. Именно поэтому при его разрушении пациенты предъявляют жалобы на ухудшение зрения в темноте. Причины пигментной дистрофии сетчатки до сих пор неизвестны, наблюдается семейно-наследственная передача заболевания. Дебют пигментной дистрофии приходится на молодой возраст. Морфологическим признаком является поражение нейроэпителиального слоя сетчатки с разрушением светочувствительных элементов (палочек и колбочек ). При этом сам пигментный эпителий набухает и смещается во внутренние слои сетчатки, параллельно происходит фиброз ретинальных сосудов. Заболевание протекает длительно с постепенной потерей зрения .Симптомами пигментной дистрофии сетчатки являются:
- отложение пигмента в сетчатке;
- атрофия (разрушение ) зрительного нерва;
- сужение полей зрения;
- потеря зрения с наступлением сумерек.
Дистрофия макулы (центральная дистрофия )
Макула – это центральная часть сетчатки, отвечающая за центральное зрение. Дистрофия макулы (макулодистрофия ) чаще всего бывает возрастная, то есть развивается у лиц старшей возрастной группы. Наряду с катарактой и глаукомой данная патология является одной из наиболее частых причин слепоты у лиц старше 60 лет. В Российской Федерации частота данной патологии составляет более 15 человек на тысячу населения, то есть каждый 20 россиянин подвержен старческой слепоте вследствие макулодистрофии.Основным симптомом макулодистрофии является утрата центрального зрения. Поражение макулы приводит к появлению зрительных иллюзий, таких как искажение линий, предметов или появление пятен в поле зрения. Выделяют две формы дистрофии макулы - «сухую» и «влажную».
Сухая форма дистрофии макулы
Является наиболее распространенной и встречается примерно в 90 процентах случаев. Она характеризуется накоплением продуктов обмена клеток, которые снижают доступ для кислорода и питательных веществ к фоторецепторам (колбочкам
). Часто этот вид макулодистрофии протекает бессимптомно. Но по мере накопления продуктов обмена в сетчатке появляются такие симптомы как «затуманивание» зрения и выпадение участков из поля зрения. Прогноз при данной форме дистрофии относительно благоприятный, так как высокая острота зрения сохраняется на протяжении многих лет.
Влажная форма дистрофии макулы
Эта форма встречается значительно реже предыдущей, приблизительно в 10 процентах случаев. Однако протекает она более злокачественно с быстро прогрессирующей потерей зрения. При влажной форме отмечается процесс «неоваскуляризации сетчатки», для которого характерно врастание новых сосудов в сетчатку. Через эти новые и неполноценные кровеносные сосуды кровь просачивается в толщу ткани. В результате этого развивается отек сетчатки и резкое ухудшение зрения. Влажная форма характеризуется более стремительным течением и неблагоприятным прогнозом. За несколько недель или месяцев происходит снижение остроты зрения вплоть до полной слепоты.
Ранние признаки заболевания
Важно знать, что при макулярной дистрофии страдает центральное и цветное зрение, поэтому, сначала происходит утрата яркости и контрастности цветов. Это может проявляться в искажении очертаний, нередко пациенту требуется большая освещенность помещения, чем ранее. Далее возникают трудности при чтении - могут выпадать отдельные буквы, слоги или даже слова. Позднее снижается острота зрения, у пациента возникают трудности как на близком расстоянии, так и при взгляде вдаль. Если не обратиться к врачу на данном этапе, то перед глазами появляется полупрозрачное пятно, которое резко снижает зрение.
Кольцевидная дегенерация сетчатки
При кольцевидной дегенерации сетчатки вокруг желтого пятна появляются мелкие точечные белые очаги. Эти очаги формируют скопления в виде колец или полуколец, отсюда и название дистрофии. Кроме колец на сетчатке визуализируются мелкие кровоизлияния. Заболевание развивается медленно, но острота зрения зависит от выраженности изменений.
Дистрофия роговицы
Роговица – это передняя часть фиброзной оболочки глаза. У здорового человека роговица гладкая, прозрачная, не содержит в себе сосудов. В строении роговицы различают пять слоев. Дистрофия роговицы – это патология, при которой прозрачность роговицы снижается, что обуславливает снижение остроты зрения.Различают первичные (врожденные ) и вторичные (приобретенные ) дистрофии роговицы. Для первичных дистрофий характерно ранее развитие заболевания, наследственный характер, медленно прогрессирующие течение. Как правило, при врожденных дистрофиях поражаются одновременно оба глаза, отчего патологический процесс носит двухсторонний и симметричный характер. Причины этих дистрофий неизвестны, а воспалительный элемент для них не характерен.
В зависимости от места поражения выделяют несколько видов дистрофий.
Видами дистрофии роговицы являются:
- эпителиальные дистрофии;
- дистрофии мембраны Боумена;
- стромальные дистрофии;
- эндотелиальные дистрофии.
Данный вид дистрофии встречается крайне редко. Это наследственная патология, которая проявляется в первые годы жизни. Одновременно поражаются оба глаза. Основными симптомами дистрофии является формирование в центральной части роговицы множества мелких пузырьков (кист ). С течением времени пузырьки превращаются в помутнения, в результате чего роговица перестает быть прозрачной. Снижение прозрачности роговицы обуславливает утрату зрения.
Дистрофия мембраны Боумена
Это также наследственно обусловленная дистрофия, которая проявляется в первые десять лет жизни ребенка. К ранним симптомам дистрофии относится светобоязнь и покраснение конъюнктивы. Морфологическим признаком является формирование мелких эрозий (язв
) в роговице, в результате чего капсула мутнеет и становится шероховатой. Вследствие этого чувствительность роговицы снижается, а острота зрения падает.
Стромальная дистрофия
Этот вид дистрофии проявляется в возрасте 10 – 15 лет. Течение заболевания медленно прогрессирующее, к 40 годам острота зрения существенно падает. Для стромальной дистрофии характерно формирование в поверхностных слоях роговицы мелких включений. Под микроскопом эти включения напоминают «крошки хлеба» или «снежинки». Чем больше таких включений, тем мутнее становится роговица, и тем больше снижается острота зрения.
Эндотелиальная дистрофия
Это очень редкий вид дистрофии, для которого характерны обширные очаги «облысения» эндотелия. Роговица отекает и приобретает серо-голубой цвет.
Лечение дистрофии сетчатки и роговицы
Лечение дистрофии сетчатки включает сосудорасширяющиеДистрофия – это патология, которая вызвана хроническими нарушениями питания и сопровождается атрофией тканей. Дистрофия может встречаться у людей в любом возрасте, но больше всего это заболевание опасно для детей в первые годы жизни. Болезнь в раннем возрасте приводит к задержке интеллектуального и физического развития, снижению иммунитета, нарушениям процессов обмена. Тяжелые и средние формы дистрофии нечасто отмечаются в социально благополучных регионах.
Дистрофия не всегда выражается дефицитом веса человека относительно его роста, как это характерно для всех пациентов-гипотрофиков. Во время другого вида – паратрофии, отмечается преобладание веса человека над его ростом и появление ожирения. Равномерное отставание и веса человека, и роста относительно возрастных норм – это еще одна разновидность дистрофии гипостатурного типа. Самая распространенная и опасная первая разновидность болезни – гипотрофная дистрофия .
Причины дистрофии
В пренатальном периоде первичная алиментарная дистрофия вызывается патологиями внутриутробной гипоксией плода и плацентарного кровообращения. К основным факторам риска при беременности относятся:
- инфекционные болезни в любом триместре;
- возраст женщины до 18 и после 45 лет;
- патологии плаценты;
- тяжелые соматические болезни, в том числе наследственные и хронические заболевания, травмы;
- курение;
- неблагоприятная социальная среда, которая приводит к нерациональному питанию и нервным стрессам;
- токсикозы или гестозы в любом триместре.
Приобретенная первичная дистрофия может являться следствием недостаточного питания в сложных социальных условиях или результатом некачественного питания с дефицитом белка. Также к первичной дистрофии приводят повторяющиеся инфекционные болезни, которые вызваны рецидивирующим отитом, ротавирусными и кишечными инфекциями.
Вторичная дистрофия пост- и пренатального периода сопровождает приобретенные и врожденные:

Развитие паратрофии, как правило, соотносят с чрезмерной калорийностью пищи и повышенным количеством в дневном меню жиров и углеводов. Появление паратрофии провоцирует диатез экссудативно-катарального и лимфатико-гипопластического видов с покраснением и воспалением слизистых оболочек и эпителия, а также с ростом лимфоидной ткани. Дистрофия гипостатурного типа сопровождается серьезными патологиями нейроэндокринной системы.
На сегодняшний день в медицинской практике существует несколько разных классификаций дистрофических состояний. С учетом того, какие разновидности нарушения обменных процессов преобладают, выделяют следующие виды дистрофии:
- углеводную;
- минеральную;
- белковую;
- жировую.
По месту локализации процесса патологии обменных процессов дистрофия может быть клеточной, внеклеточной и смешанной.
По этиологии дистрофия бывает:
- Приобретенная. Появляется под действием внешних или внутренних факторов и имеет более благоприятный прогноз, в отличие от врожденных форм.
- Врожденная. Развитие патологии связано с генетическими факторами, то есть дисфункция обменных процессов белков, углеводов и жиров связана с наследственной патологией. Причем в организме детей нет одного или нескольких ферментов, которые ответственны за метаболизм питательных элементов. В итоге происходит неполноценное расщепление углеводов, жиров или белков, а в тканях происходит скопление продуктов метаболизма, которые губительно действуют на структуры клеток. Патология затрагивает самые разные ткани, но чаще всего поражается нервная ткань, это приводит к серьезному нарушению ее функционирования. Любые разновидности врожденной дистрофии относятся к опасным состояниям, которые способны привести к летальному исходу.
С учетом дефицита массы тела дистрофии делят на такие группы:
- Гипостатруа. Характеризуется не только недостатком массы тела, но и снижением роста, не соответствие данных показателей возрастным нормам.
- Паратрофия. При таком виде дистрофии нарушения питания тканей и обменных процессов приводит к повышению массы тела.
- Гипотрофия. Сегодня это самый часто встречающийся вид заболевания. При этом отмечается снижение веса относительно роста человека. С учетом от момента появления классифицируют врожденную (пренатальную), приобретенную (постнатальную) и комбинированную гипотрофию.
Когда дистрофия появляется в результате нехватки белков, углеводов (энергетических веществ) или жиров, то она называется первичной. Вторичную дистрофию рассматривают в случаях, если патология появляется на фоне какого-то другого заболевания.
 Гипотрофия на первом этапе выражается дефицитом массы тела примерно 15-22% относительно физиологической нормы. Состояние человека – удовлетворительное, с небольшим уменьшением подкожных жировых отложений, снижением тургора кожи и аппетита
.
Гипотрофия на первом этапе выражается дефицитом массы тела примерно 15-22% относительно физиологической нормы. Состояние человека – удовлетворительное, с небольшим уменьшением подкожных жировых отложений, снижением тургора кожи и аппетита
.
На втором этапе гипотрофии с дефицитом веса человека до 30% у больного понижена двигательная активность и эмоциональный тонус. Пациент – апатичен, тургор тканей и мышечный тонус значительно понижен. У человека сильно снижено количество жировой клетчатки в районе конечностей и живота. Патологии терморегуляции выражены в холодных конечностях и колебания температуры тела. Дистрофия на второй стадии сопровождается патологиями в работе сердечнососудистой системы с артериальной гипотензией, тахикардией, приглушенностью сердечных тонов.
Гипотрофию на третьей стадии с дефицитом веса человека больше 30% также называют алиментарным маразмом или атрофией . На этом этапе развития болезни общее состояние человека серьезно нарушено, пациент склонен к безучастности, сонливости, анорексии, раздражительности. При гипотрофии на третьей стадии нет жировой подкожной клетчатки. Мускулатура полностью атрофирована, но мышечный тонус повышен из-за расстройств электролитного баланса и присутствия неврологических нарушений. Гипотрофия сопровождается пониженной температурой тела, обезвоживанием, слабым и редким пульсом, артериальной гипотензией. Дискинетические проявления дистрофии выражаются в рвоте, срыгивании, редком мочеиспускании, учащенном жидком стуле.
Гипостатура – это следствие пренатальной дистрофии нейроэндокринного вида. Диагностируется врожденная гипостатура во время рождения ребенка по отличительным клиническим симптомам:

Врожденные устойчивые нарушения нервной и эндокринной регуляции процессов плохо поддаются лечению. Во время отсутствия вышеперечисленных клинических симптомов и одновременно присутствующим отставанием физиологических показателей роста и веса человека от возрастных норм гипостатура может являться результатом конституциональной низкорослости.
У детей чаще всего паратрофия провоцируется чрезмерным приемом пищи или несбалансированным питанием с недостаточным содержанием белка и большим количеством углеводов. Более склонны к паратрофии неактивные дети на искусственном кормлении с разными видами диатеза. Систематичная гиподинамия и продолжительное перекармливание часто развивают ожирение, как один из симптомов дистрофии паратрофического вида. Также клиническими симптомами паратрофии являются:
- вялость;
- нарушенный эмоциональный тонус;
- быстрая утомляемость;
- одышка;
- боли в голове.
Зачастую аппетит понижен и носит избирательный характер. Из-за избыточной жировой подкожной клетчатки отмечается сниженный тонус мышц и недостаточная эластичность покровов кожи. На фоне снижения иммунитета вероятны функциональные и морфологические трансформации внутренних органов.
Диагностика дистрофии
 Установление диагноза «дистрофия» производится на основании клинических характерных симптомов, которые включают соотношение веса человека относительно роста, анализ сопротивляемости организма к инфекционным болезням, размещение и количество жировой подкожной клетчатки, оценка тургора тканей. Стадия гипотрофии определяется по данным лабораторных обследований мочи и крови.
Установление диагноза «дистрофия» производится на основании клинических характерных симптомов, которые включают соотношение веса человека относительно роста, анализ сопротивляемости организма к инфекционным болезням, размещение и количество жировой подкожной клетчатки, оценка тургора тканей. Стадия гипотрофии определяется по данным лабораторных обследований мочи и крови.
Гипотрофия на первой стадии - лабораторные обследования желудочной секреции и крови указывают на диспротеинемию, которая выражается в пониженной активности пищеварительных ферментов и дисбалансе фракций белков крови.
Гипотрофия на второй стадии - по данным лабораторных обследований у человека с дистрофией на этом этапе сильно выражена гипохромная анемия с пониженным содержанием в крови гемоглобина. Также отмечается гипопротеинемия с низким количеством в крови общего белка на фоне сильного уменьшения ферментной активности.
Гипотрофия на третьем этапе - лабораторные обследования указывают на присутствие в моче значительных количеств хлоридов, фосфатов, мочевины, в некоторых случаях кетоновых тел и ацетона, а также сгущение крови с медленным оседанием эритроцитов.
Дифференционный диагноз «гипостатура» определяется с помощью исключения болезней, которые сопровождаются отставанием физического развития, к примеру, гипофизарного нанизма, во время которого гипофиз человека не синтезирует необходимого количества соматотропных гормонов, либо иных мутационных видов нанизма с нормальной секрецией соматропина, но не чувствительностью организма к нему.
Диетотерапия является основополагающим аспектом рационального лечения дистрофии. Изначально определяется переносимость организмом пищи , при необходимости рекомендуются ферменты: фестал, абомин, панкреатин, панзинорм. На последующем этапе производится постепенная корректировка энергетической ценности и объема потребляемой пищи с постоянным контролем убавления или набора массы тела, диуреза и характера стула. Для этого заводится пищевой журнал с занесением наименований и количества продуктов. Питание происходит небольшими порциями до 7-12 приемов пищи в день. Контроль производится до достижения человеком физиологических норм массы тела.
В качестве стимулирующего лечения используют курсы общетонизирующих препаратов и мультивитаминные комплексы: препараты с маточным молоком, женьшенем, овсом, лимонником. Также производится лечение сопутствующих болезней и санирование очагов хронической инфекции . Повышение эмоционального статуса и устранение гиподинамии достигается с помощью массажа, комплексного выполнения физических лечебных упражнений.
 Пренатальные профилактические мероприятия, которые направлены на предупреждение появления внутриутробной дистрофии, в себя включают: режим отдыха и работы, полноценный сон, физические посильные упражнения, сбалансированное питание, постоянный мониторинг состояния здоровья плода и женщины, контроль веса женщины.
Пренатальные профилактические мероприятия, которые направлены на предупреждение появления внутриутробной дистрофии, в себя включают: режим отдыха и работы, полноценный сон, физические посильные упражнения, сбалансированное питание, постоянный мониторинг состояния здоровья плода и женщины, контроль веса женщины.
У ребенка постнатальная профилактика дистрофии лучшим образом проводится при естественном кормлении , регулярном контроле над ежемесячными прибавлениями веса и роста на протяжении первого года и ежегодном контроле последующей динамики физического развития.
У взрослых пациентов предупреждение дистрофии возможно с условием нормального питания, лечения основных иммунодефицитных заболеваний, а также заместительной терапии мальабсорбции и энзимопатии.
Необходимо понимать, что укрепление своего иммунитета, а также иммунитета ваших детей с самого рождения, сбалансированное, рациональное и здоровое питание, отсутствие стрессов и достаточные физические нагрузки – это наилучшая профилактика любых заболеваний и в том числе дистрофии.